口腔鳞状细胞癌(OSCC)是最常见的口腔恶性肿瘤,其转移是患者预后差的主要原因。自噬可通过减轻各种细胞应激促进OSCC的发展。然而,自噬在OSCC细胞增殖和转移中的作用机制尚不清楚。
2022年4月25日,上海交通大学张志愿教授团队、浙江大学周舟教授团队和陆军军医大学皮会丰教授团队合作在Signal Transduction and Targeted Therapy(IF 18.187)上发表了题为“NUPR1 promotes the proliferation and metastasis of oral squamous cell carcinoma cells by activating TFE3-dependent autophagy”的研究论文,该研究使用Labelfree定量蛋白组学方法分析显示,核蛋白 1 (NUPR1) 是有或无淋巴转移OSCC患者的福尔马林固定石蜡包埋(FFPE)肿瘤样本中最显著上调的蛋白,NUPR1 在 OSCC 组织中异常表达,可能与 OSCC 患者的总体存活率较低。此外该研究使用TMT标记定量蛋白组学方法分析显示NUPR1通过直接增加转录因子E3 (TFE3)活性来维持自噬流和溶酶体功能,进而促进 OSCC 细胞增殖和体内外转移。本研究中NUPR1-TFE3介导的自噬过程为靶向OSCC进展的药物治疗提供了潜在的治疗靶点。中科新生命为本研究提供了Labelfree非标记定量蛋白组学和TMT标记定量蛋白组学的技术支持。

研究材料
有和无淋巴转移的OSCC的FFPE样本、Cal27和HN6癌细胞系、OSCC组织和正常粘膜组织
技术路线
1. Labelfree蛋白组学分析发现NUPR1在有淋巴转移的OSCC的FFPE样本中显著上调
作者首先对来自有淋巴转移(LNM)和没有淋巴转移(non-LNM)的OSCC患者的FFPE肿瘤样本(分别为10个样本)进行了Labelfree非标记定量蛋白组学分析(图1a)。此次共鉴定到3021个蛋白,LNM vs non-LNM组的比较分析显示208个蛋白显著上调,其中NUPR1蛋白是上调倍数前五的蛋白(图1c)。
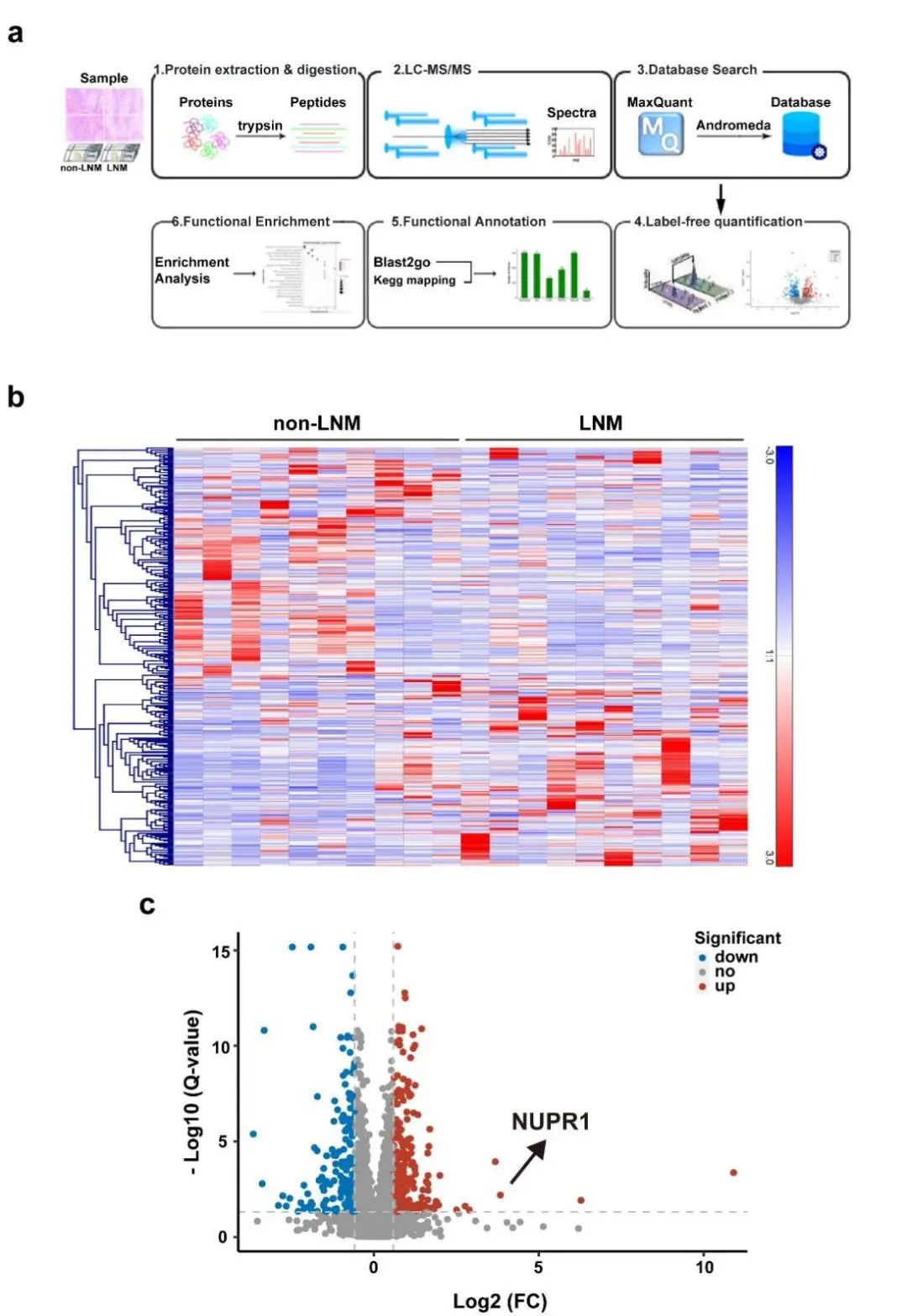
图1 Labelfree非标记定量蛋白组学分析
2. NUPR1与患者的OSCC进展及不良预后呈正相关
为验证蛋白组学的结果,作者采用IHC的方法进行了NUPR1的组织芯片(TMA)实验,结果表明NUPR1表达水平在OSCC组织中(n = 88)相较于正常粘膜组织(n = 20) 显著增加(图2a和2c)。NUPR1表达水平与临床病理特征的关联分析表明NUPR1与OSCC转移呈正相关(图2b、2d和2e)。此外,Kaplan-Meier生存分析显示NUPR1高表达的OSCC患者总生存率较低(图2f)。
为了进一步阐明NUPR1在OSCC进展中的作用,作者在高表达NUPR1的OSCC细胞系(Cal27和HN6癌细胞系)中将NUPR1敲除。集落形成实验显示,NUPR1敲低后显著降低了OSCC癌细胞的集落形成效率(图2g)。伤口愈合和Transwell侵袭实验结果表明NUPR1敲低的癌细胞迁移和侵袭能力明显受到抑制(图2h-2j)。综上所述,NUPR1 敲低有效地抑制了OSCC的进展,表明了NUPR1与OSCC的进展的正相关性。
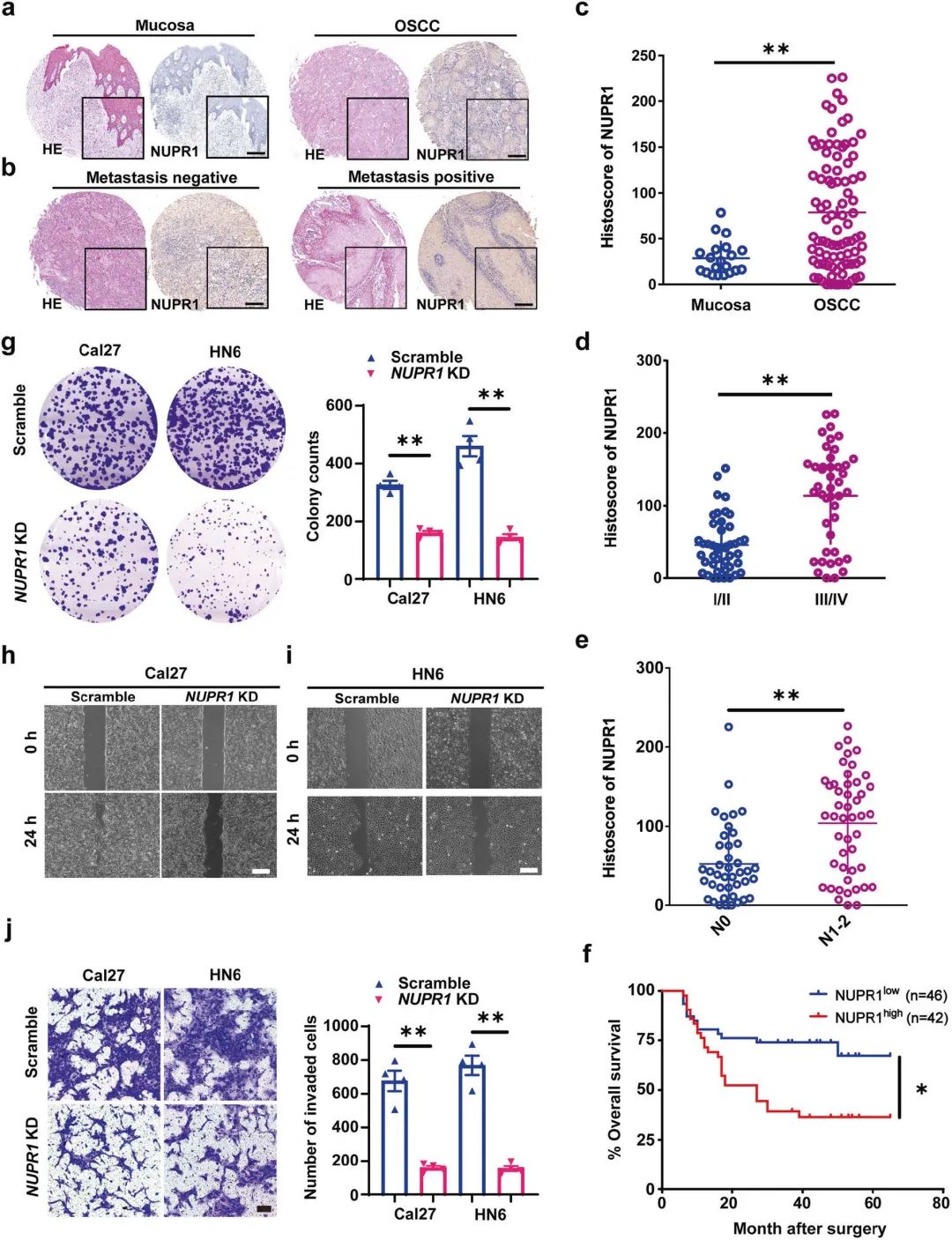
图2 NUPR1与OSCC进展及不良预后呈正相关
3. 蛋白组学揭示自噬在NUPR1介导的OSCC进展中发挥重要作用
为了揭示NUPR1在OSCC进展中的潜在机制,作者采用TMT标记定量蛋白组学的方法检测了NUPR1敲低的Cal27癌细胞和对照组细胞间的蛋白变化。比较分析显示与对照组相比,NUPR1敲低的Cal27癌细胞中27个蛋白显著上调、28个蛋白显著下调(图3a)。差异蛋白的KEGG通路富集分析表明,自噬通路显著富集(图3b),这意味着自噬可能在NUPR1介导的OSCC进展中发挥重要作用。
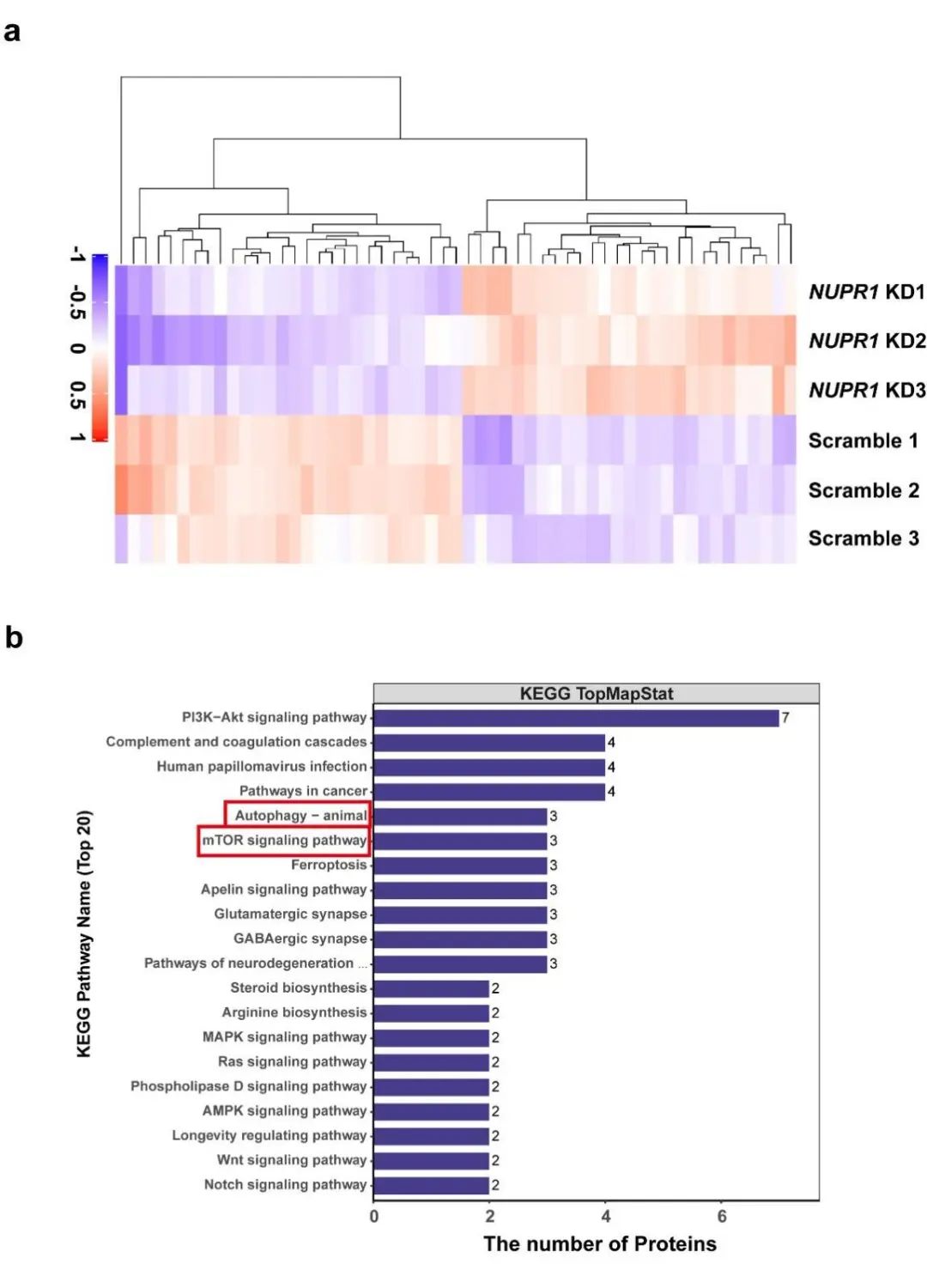
图3 自噬在NUPR1介导的OSCC进展中发挥重要作用
4. NUPR1的敲低阻断了OSCC细胞中的自噬流
为验证NUPR1的敲低是否影响OSCC细胞中的自噬流,作者分析了自噬体形成的标志物MAP1LC3B-II(微管相关蛋白轻链3)的变化,结果显示在Cal27和HN6癌细胞将NUPR1敲低后,MAP1LC3B-II表达水平均增加(图4a和4b),以及SQSTM1(选择性自噬接头蛋白)的表达水平也明显增加(图4a和4b)。然而在癌细胞中将NUPR1敲低同时加入氯喹(CQ)(自噬以及自噬流的抑制剂)时,NUPR1敲低诱导的MAP1LC3B-II的表达增加不受影响(图4c和4d)。综上所述,在OSCC细胞中,NUPR1的敲低可抑制自噬流。
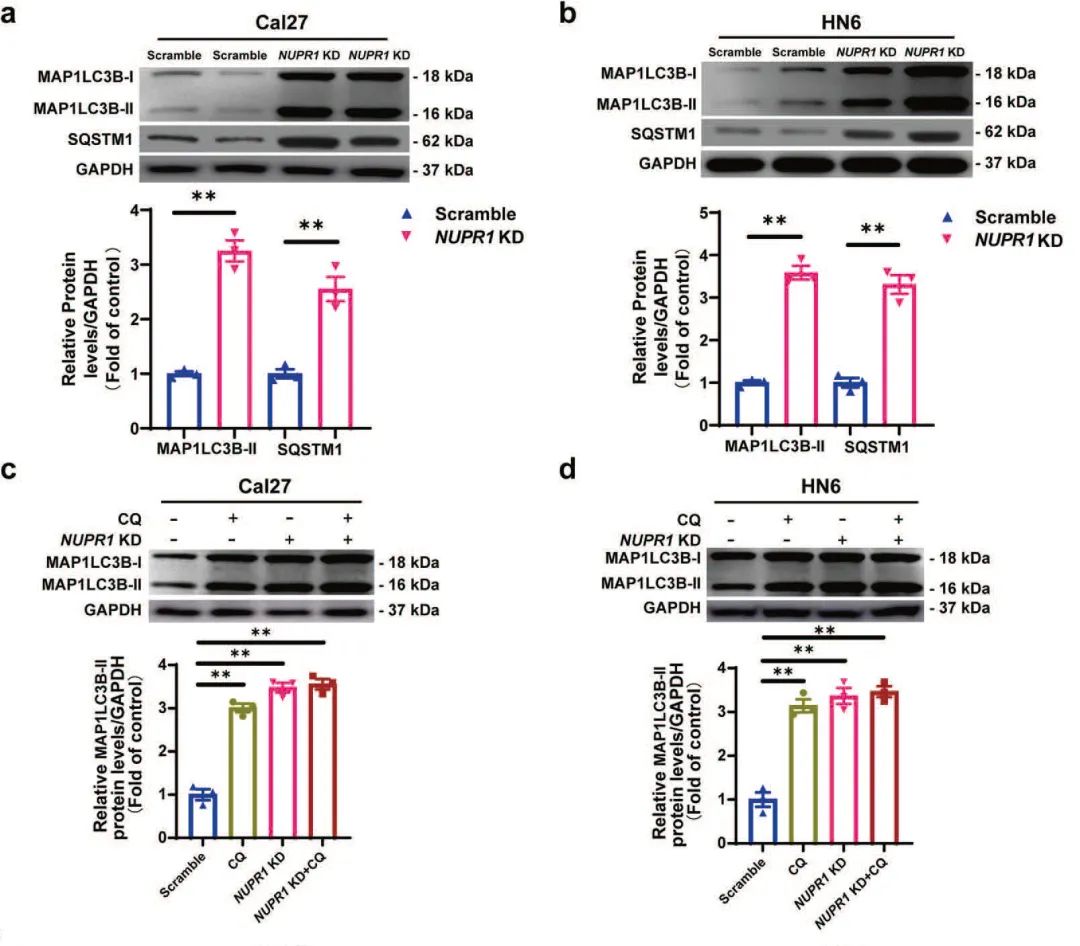
图4 NUPR1的敲低阻断了OSCC细胞中的自噬流
5. NUPR1的敲低不抑制OSCC细胞自噬体的形成和成熟
由于自噬是一个动态循环系统,具有多个步骤(①自噬泡的形成②Atg5-Atg12-Atg16L复合物形成并与自噬泡融合③微管相关蛋白轻链3(LC3)与自噬泡结合形成自噬体④自噬体捕获需降解或清除的蛋白质等物质⑤自噬体与溶酶体结合形成自噬溶酶体、内容物降解),作者进一步研究了NUPR1敲低在早期或晚期诱导的自噬抑制作用。研究发现ATG5 沉默降低了NUPR1敲低诱导的Cal27和HN6细胞GFP-LC3(自噬体的特异性标记物)的增加(图5a和5b),也降低了MAP1LC3B-II的积累(图5c和5d),表明NUPR1的敲除不影响自噬体的形成。多泛素蛋白聚集物是成熟自噬体的重要组成部分,其形成是由SQSTM1介导的,作者通过评估GFP-LC3与SQSTM1的共定位来评估自噬小体的成熟。结果表明NUPR1的敲低并不促进OSCC细胞中自噬体的成熟(图5e和5f)。
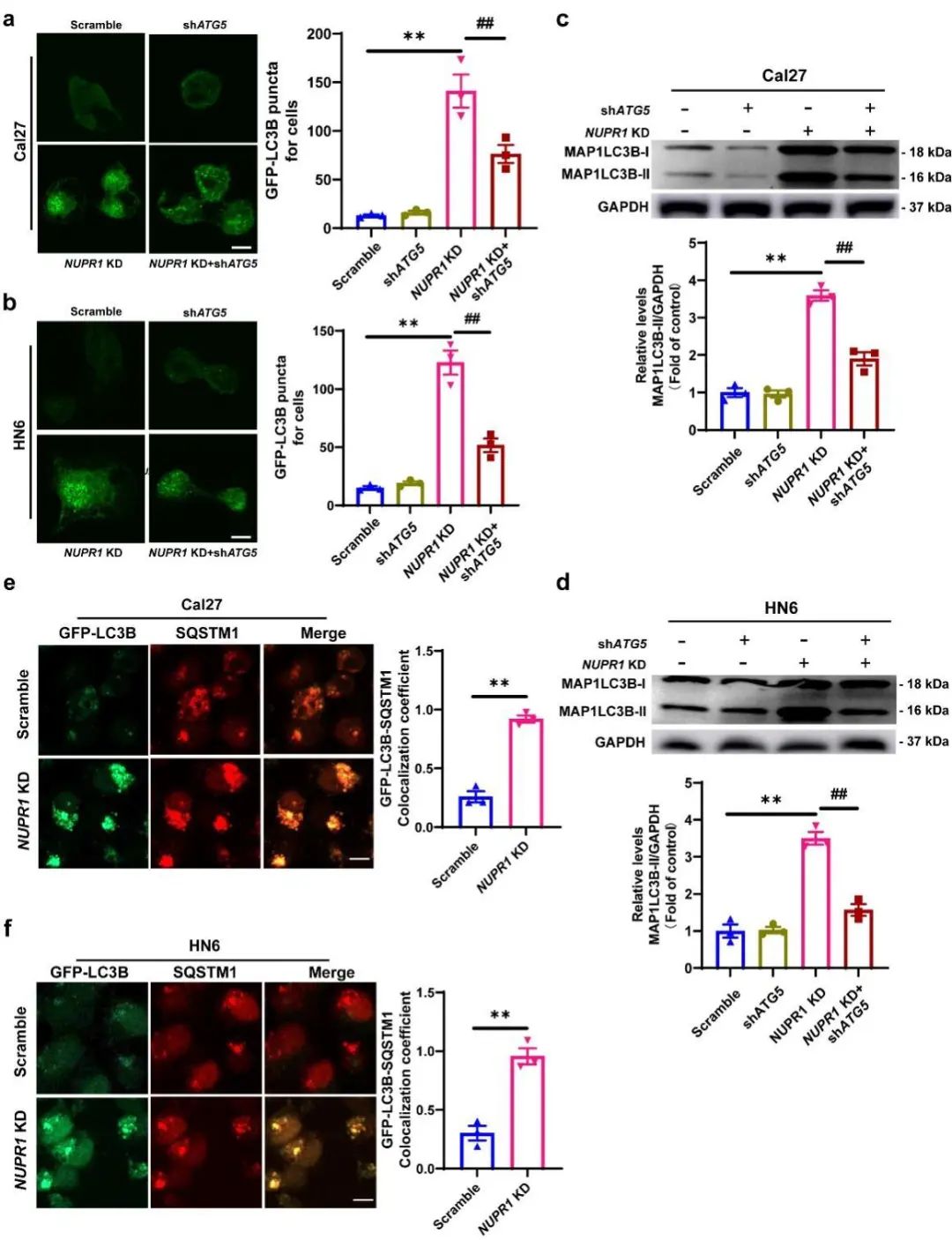
图5 NUPR1的敲低不抑制OSCC细胞自噬体的形成和成熟
6. NUPR1敲低不影响OSCC细胞中的自噬体-溶酶体的融合
自噬体与溶酶体的融合是自噬降解的一个基本过程,研究发现在Cal27和HN6细胞中,自噬体标记物GFP-LC3和溶酶体标记物LAMP2的共定位比例不受NUPR1敲低的影响(图6)。
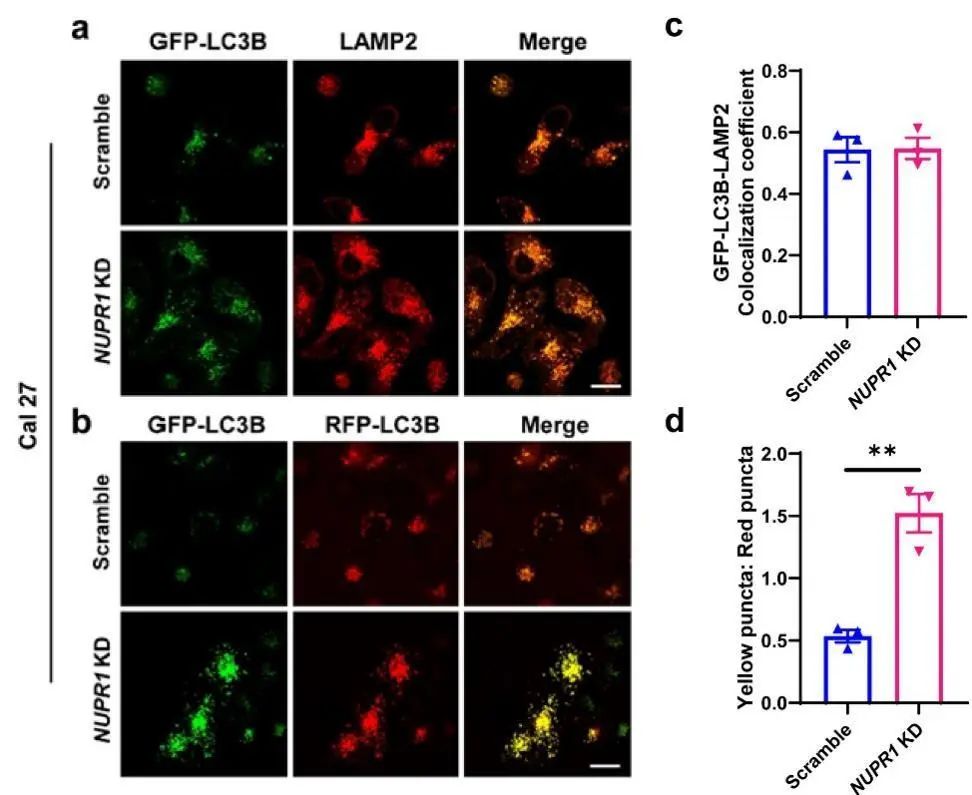
图6 NUPR1敲低不影响OSCC细胞中的自噬体-溶酶体的融合
7. NUPR1的敲低抑制了OSCC细胞中溶酶体的功能
为了研究NUPR1的敲低是否抑制了溶酶体的功能,作者检测了溶酶体标志物LAMP1和LAMP2的表达水平。结果表明,在Cal27和HN6细胞中,NUPR1的敲低抑制了LAMP1的表达,但不抑制LAMP2 (图7e和7f)。此外,在NUPR1敲低的OSCC细胞中,溶酶体蛋白水解活性明显受到抑制(图7g)、溶酶体绿色荧光探针的荧光强度也显著降低(图7h)。综上所述NUPR1敲低对自噬流的阻断可能是通过抑制OSCC细胞内溶酶体功能来介导的。
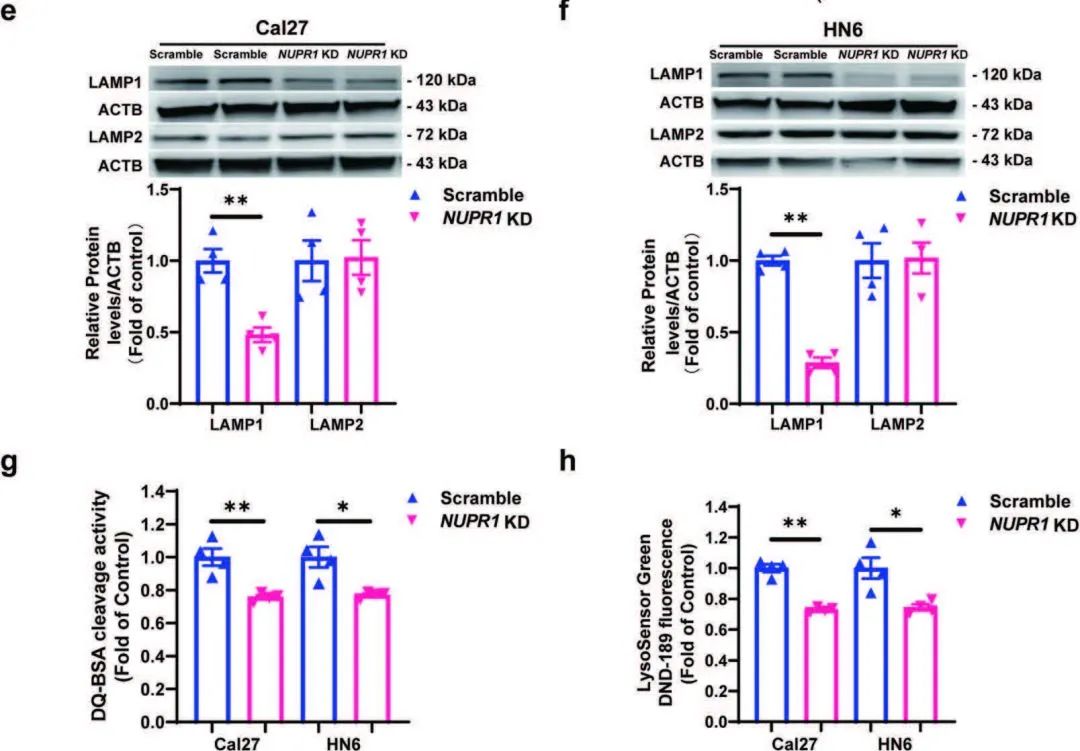
图7 NUPR1的敲低抑制了OSCC细胞中溶酶体的功能
8. TFE3负责OSCC细胞中NUPR1介导的自噬溶酶体过程
为了阐明NUPR1影响自噬溶酶体的潜在机制,作者使用蛋白质组学方法分析NUPR1敲低的Cal27细胞和对照组的显著差异蛋白,结果表明NUPR1的敲低显著降低了TFE3的表达水平,western blot实验进一步验证了该结果(图8a和8b),PCR实验也证实了自噬流中涉及的“TFE3应答基因”的表达变化(图8c和8d),综上表明NUPR1在自噬溶酶体事件中发挥的关键作用可能与TFE3有关。
已知NUPR1是调控基因转录的重要转录因子,故作者采用荧光素酶报告基因的方法检测NUPR1与TFE3的关系,结果表明在OSCC进展中,NUPR1是通过增加TFE3启动子活性和激活TFE3转录来维持自噬流的(图8e和8f)。
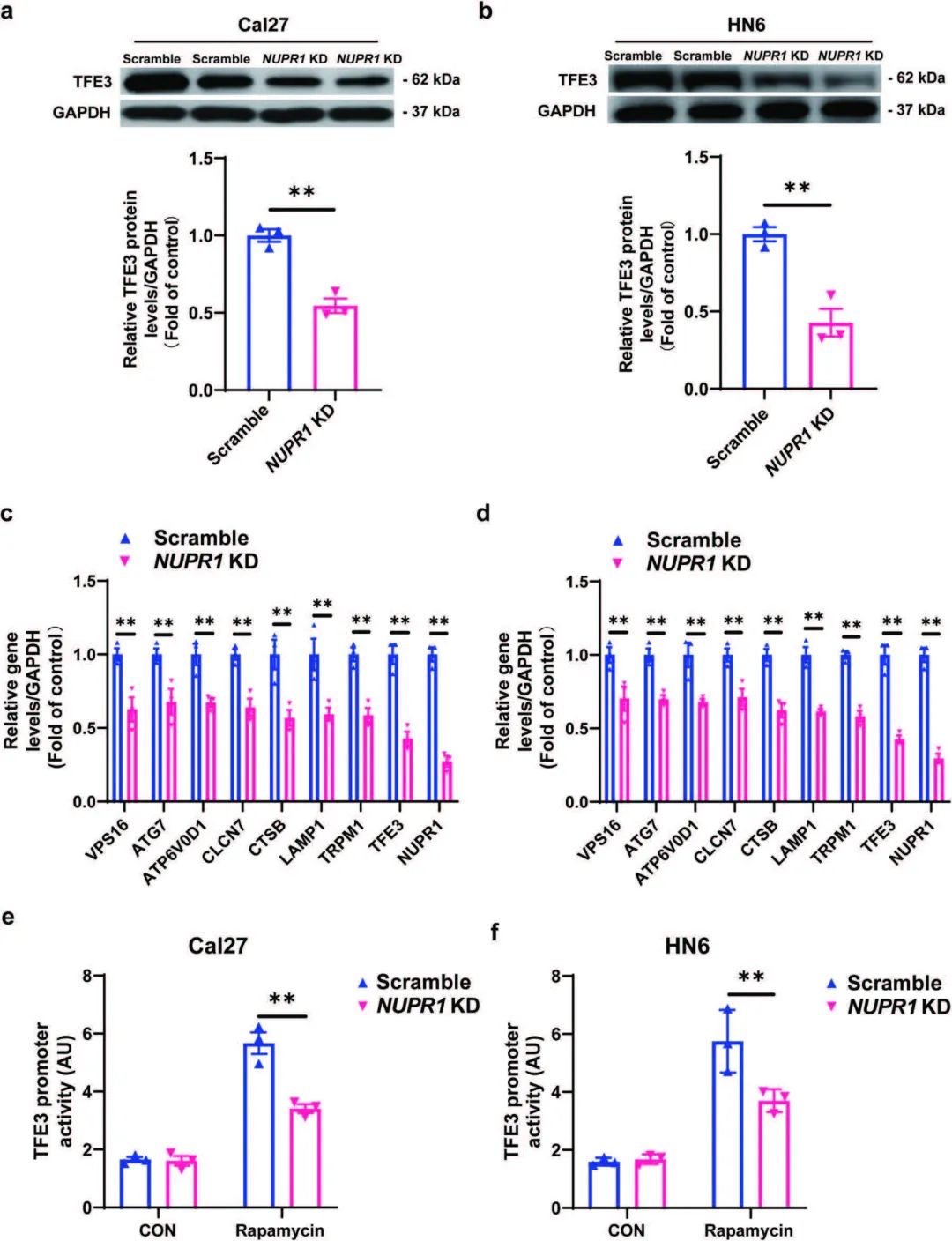
图8 NUPR1在自噬溶酶体事件中发挥的关键作用与TFE3有关
此外, TFE3的过表达可以显著挽救NUPR1敲低对Cal27和HN6细胞溶酶体功能的损伤(图9a-9d),也显著降低了NUPR1缺失的OSCC细胞中MAP1LC3B-II和SQSTM1的积累(图9e和9f)。
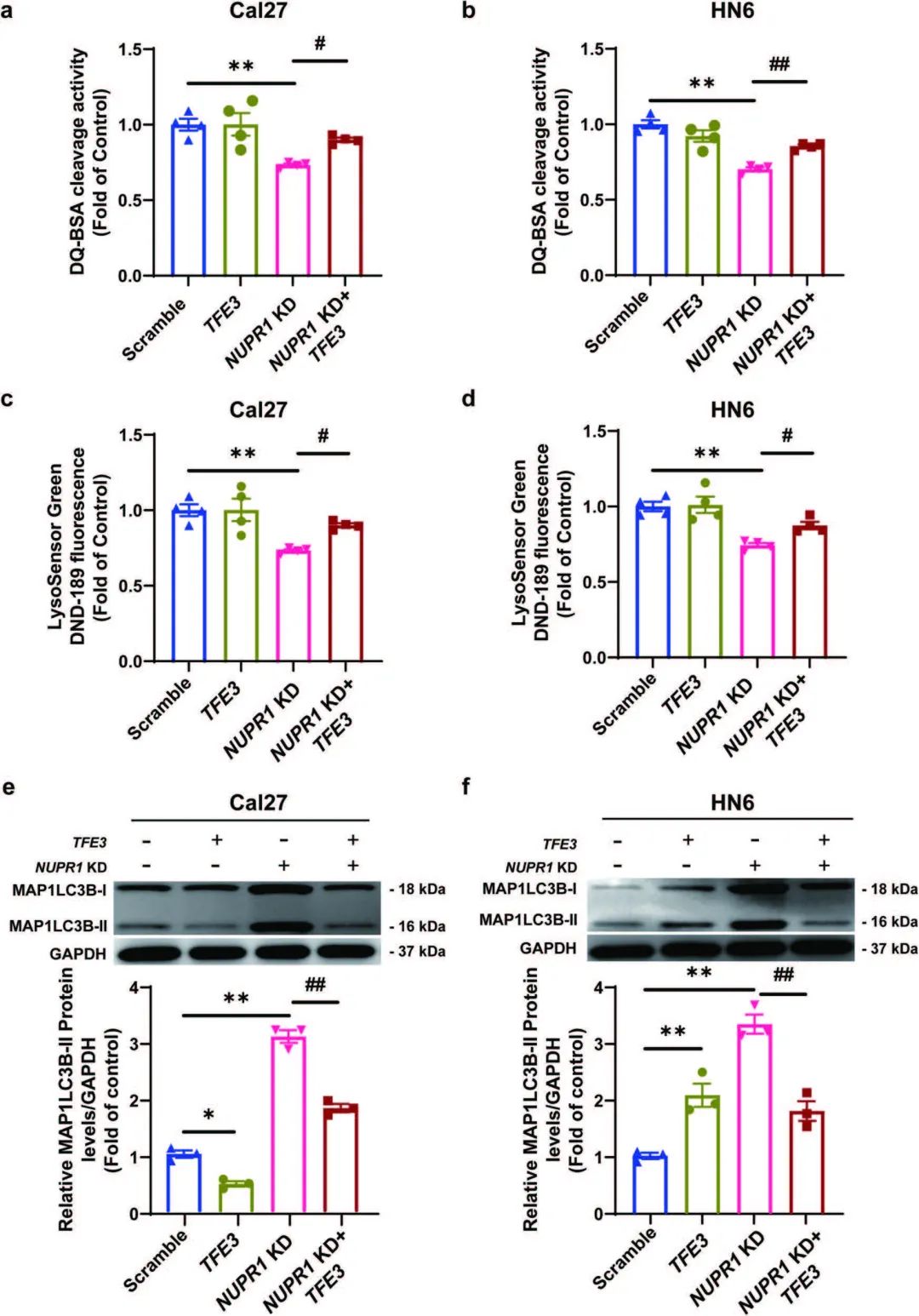
图9 TFE3过表达可挽救OSCC细胞中NUPR1 减少引起的自噬流的抑制
9. 在体外和体内,NUPR1通过激活TFE3依赖的自噬促进OSCC的进展
为了探究TFE3在NUPR1敲低介导的OSCC细胞进展中的影响,作者展开了一系列的体外实验,结果表明TFE3的过表达部分逆转了NUPR1 敲低介导的OSCC细胞迁移和侵袭的抑制作用(图10a-f)。
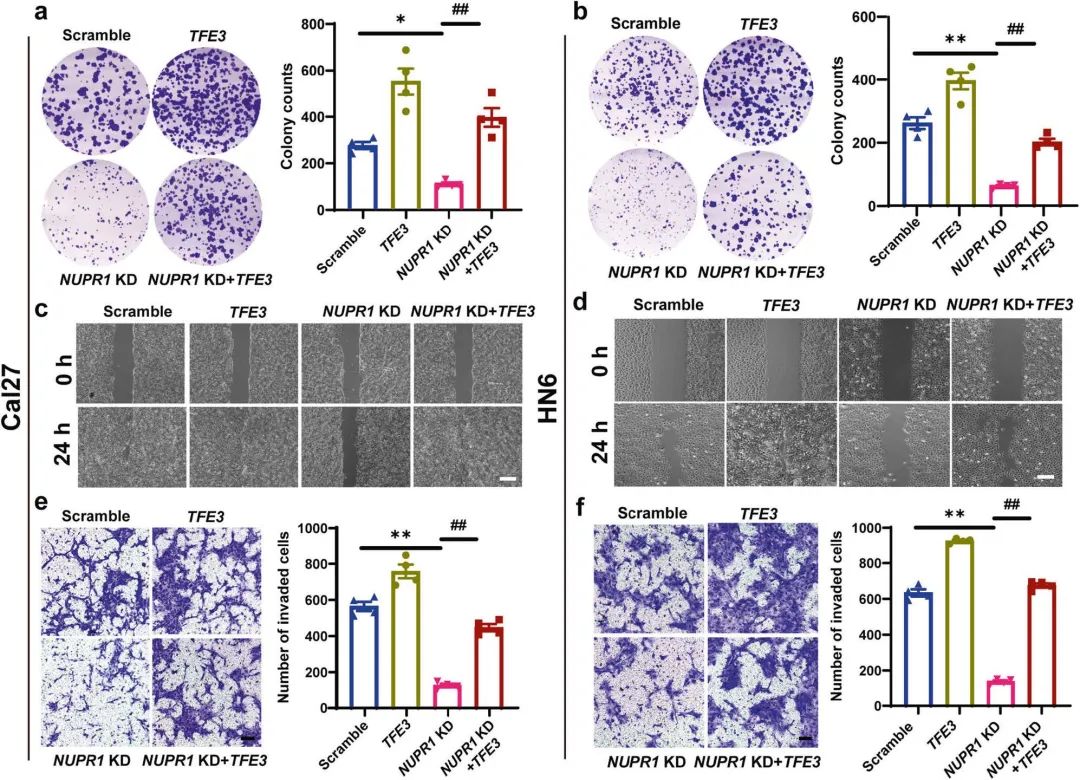
图10 TFE3的过表达可拮抗NUPR1 敲低诱导的OSCC细胞增殖和转移抑制
此外,体内实验发现NUPR1敲低导致接种于裸鼠皮下的Cal27细胞形成的肿瘤的体积和重量明显减少(图11a-11c)。也导致了转移性结节形成和生长的抑制(图11d)。同时,NUPR1敲低有效地抑制了异种移植瘤模型中TFE3和“TFE3应答基因”的表达(图11e)。在对转移性结节的评估中也得到了同样的结果(图11f)。综上所述,NUPR1敲低对OSCC进展的抑制依赖于TFE3活性的抑制。
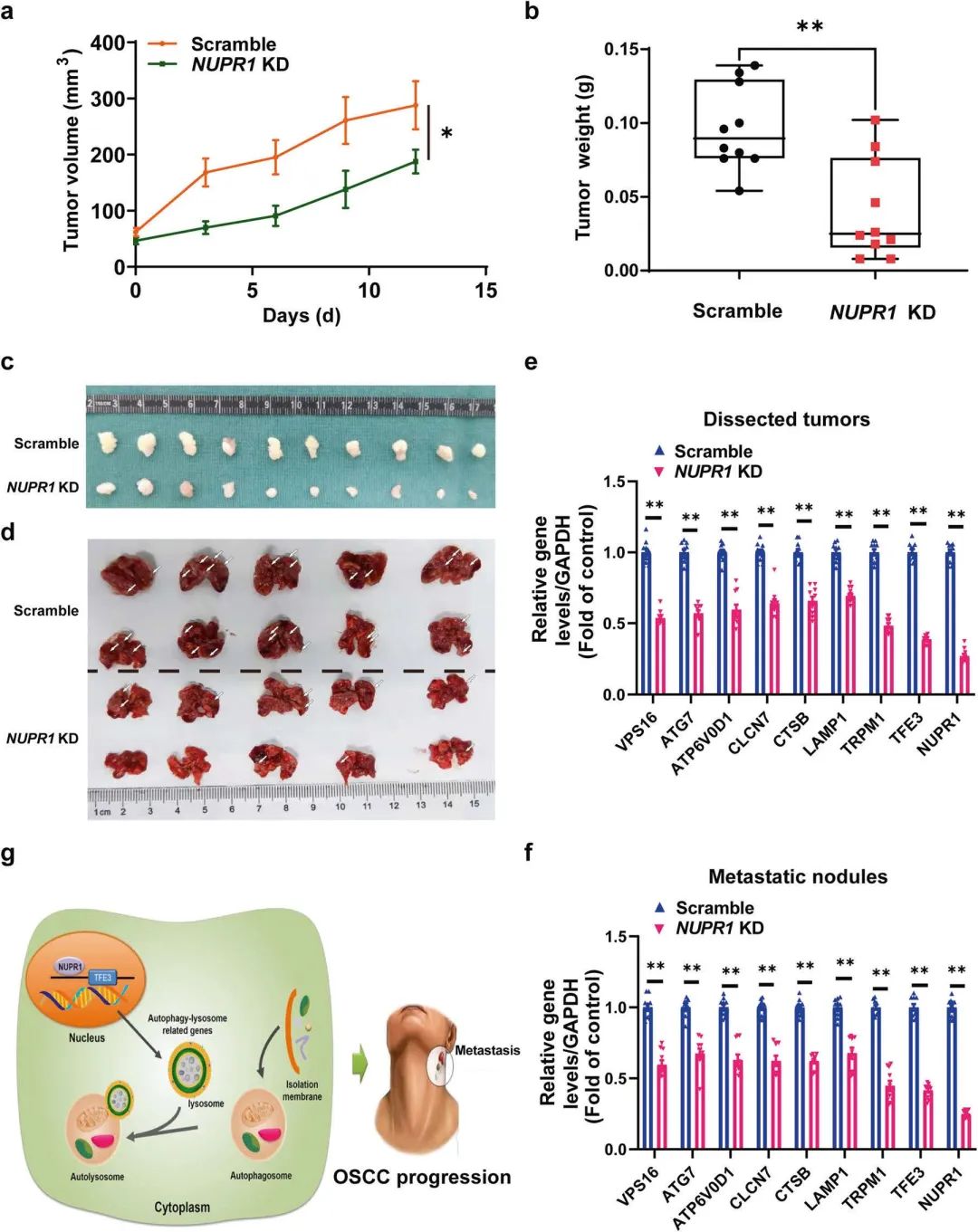
图11 NUPR1的敲除抑制了裸鼠OSCC的侵袭性
小编小结
在本研究中,作者首次证明了(Ⅰ)通过对有淋巴结转移和无淋巴结转移的口腔鳞状细胞癌 (OSCC)组织FFPE样本的蛋白组学分析发现了NUPR1是一种关键蛋白,在LNM患者中显著增强,且与OSCC转移和不良预后呈正相关。(Ⅱ)溶酶体功能障碍而非其他关键步骤的破坏(自噬体形成或成熟,自噬体-溶酶体融合)是NUPR1 敲低诱导的自噬流受损和OSCC细胞增殖和转移抑制的关键原因。(Ⅲ)在OSCC进展中,NUPR1通过增加TFE3启动子活性和激活TFE3转录来维持自噬流。这些发现为细胞癌进展中NUPR1-TFE3依赖的自噬的潜在治疗靶点拓宽了新的见解。
中科优品推荐
【中科新生命】经过18年的时间积累,现已建立起了Labelfree、TMT、4D-Labelfree、4D-DIA、4D-labelfree修饰、DIA磷酸化、外泌体多组学等多种蛋白组学平台以及代谢、转录平台。此外,中科新生命有着专业的数据分析平台以及售前售后服务团队,为老师提供全面的技术支持。欢迎感兴趣的老师前来咨询。

