友康生物在5月18日召开的第10届细胞治疗国际研讨会上,正式推出GMP级细胞冻存液,该冻存液经批准后可以回输人体。

细胞药物的应用面临一个极大的挑战,就是药物本身的保存问题。细胞药物作为继化学药,生物药后的第三类药物,其特性明显。而传统的化学药及生物药只是一种无生命的组分。作为药物的细胞,它必须是活生命体。而保存细胞的传统方式是用含DMSO的细胞冻存液保存,使用前清洗细胞(因为DMSO有毒性)。但作为药物来说,这显然不太可能:临床医生没有清洗细胞的条件,并且如果临床医生去清洗细胞(二次加工)又如何能称为药品?不清洗细胞,其中的DMSO的毒性又如何去除?
友康生物应中国著名的Car-T药物开发企业的要求(非专属开发合同,委托企业不拥有对应知识产权)开发成功了GMP级细胞冻存液。该冻存液无DMSO,无血清,无蛋白。化学成分明确。可在-80度及-196度条件下长期保存(已有8个月保存数据),复苏后的细胞活性超出90%。且细胞冻存时不需要程序降温。
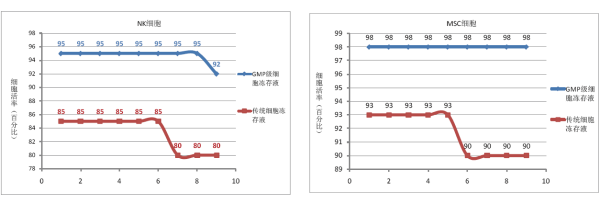
该产品作为药用辅料,已经在中国合格实验机构完成了急性毒性试验。长期毒性试验正在进展之中。

该产品作为**的创新性产品,已经申报了中国发明**,并且已经完成了在美国、欧盟、日本等国的发明**的申请。
该产品打通了细胞制剂从实验室到临床应用的“最后一公里”。科技让不可能成为可能。
