
翌圣生物重要战略合作伙伴——英百瑞(杭州)生物医药有限公司于今年9月收到国家药品监督管理局药品审评中心(CDE)发布的IBR733细胞注射液临床试验(IND)申请的受理(受理号:CXSL2300643)。
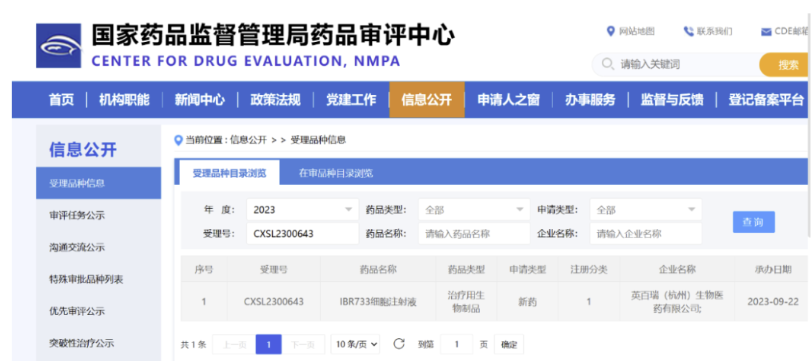
IBR733细胞注射液是同源异体外周血来源的通用现货型CAR-raNK细胞产品,主要用于治疗复发/难治急性髓系白血病。 翌圣生物在此项目中提供了全面的支原体NAT快速检测相关的技术服务与验证支持,其中MycAway™支原体qPCR检测试剂盒已根据EP 2.6.7和JP G3对其专属性、检测限和耐用性进行了全面验证,同时覆盖USP、WHO、ChP等中要求验证的支原体菌株类型,试剂盒性能符合中外法规及国际权威机构标准,助力该项目的临床实验申请顺利获得国家药监局受理。
翌圣生物相关产品: NAT法 | 支原体qPCR检测和方法验证
关于IBR733注射液
IBR733注射液是由英百瑞自主研发的一款全球创新的CD33/CLL1双特异抗体与NK细胞复合偶联的产品,其产品结构和治疗方法均为国际首创,具有重要里程碑意义。英百瑞已开展的研究者发起的临床试验(IIT)结果显示,IBR733注射液疗效显著且非常安全,有望为AML患者带来新的希望。
关于英百瑞
英百瑞致力于解决临床未满足的肿瘤和免疫类疾病的治疗,主要聚焦全球前沿的NK细胞治疗药物和细胞连接器产品的开发。英百瑞有国际独创的tiNK、CAR-raNK细胞技术平台,有国际领先的体外大规模封闭式培养NK细胞的先进工艺,基于自有平台技术开发了IBR854、IBR733等多个通用现货型细胞治疗产品,已进行多个研究者发起的临床试验(IIT),初步证明了安全性和有效性,目前IBR854细胞注射液已推进到I期临床试验阶段,另有多个实体瘤和血液瘤的新药正在逐步推进中。
