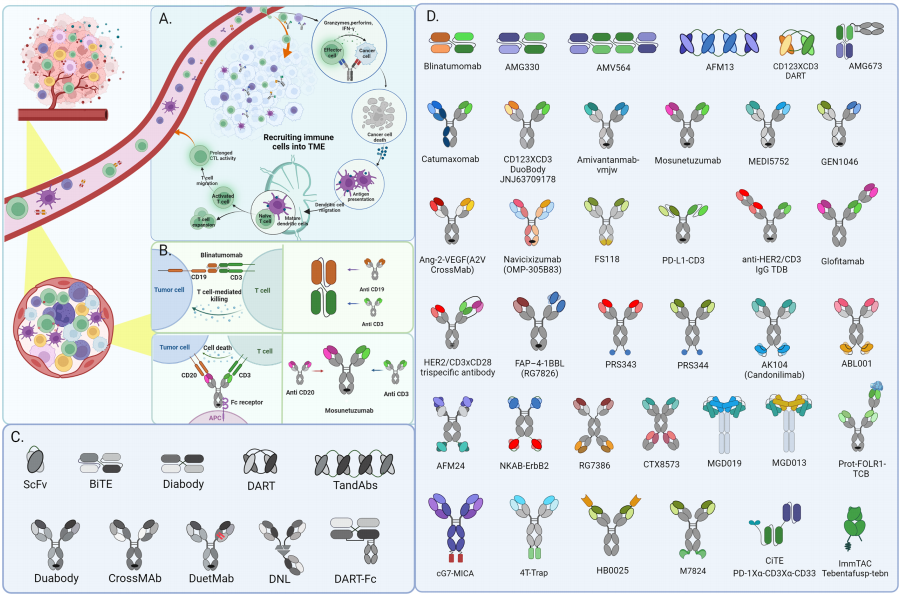
BsAbs在实体瘤(A)和血液系统恶性肿瘤(B)中的作用机制示意图
肿瘤现行双抗免疫疗法
CD3双特异性抗体
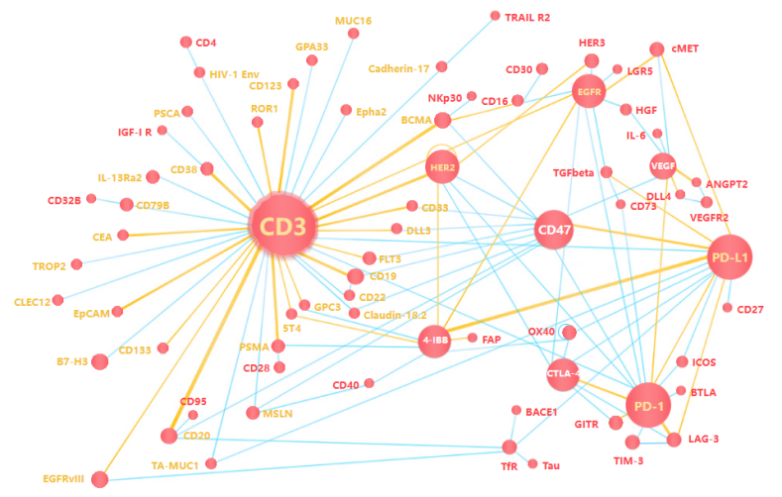
CD3-双特异性抗体(CD3-BsAbs)是癌症免疫治疗领域中一种新兴的治疗方式。CD3-BsAbs通过同时结合肿瘤细胞上表达的肿瘤相关抗原(TAA)和T细胞上的CD3发挥作用。CD3-BsAbs将这两种细胞类型交联,可以形成免疫突触,这种突触通过促进T细胞活化,从而分泌炎症细胞因子和细胞溶解分子以杀死肿瘤细胞。
【难点·痛点】CD3与实体瘤
临床研究表明,CD3-BsAbs在血液瘤中似乎比在实体瘤中更有效,可能归因于CD3-BsAbs在实体瘤领域特有的几项挑战:
痛点1:肿瘤抗原脱靶造成毒性
CD3-BsAbs可以通过TAA臂结合到健康细胞上的相同抗原,使T细胞转向正常组织,导致永久性组织破坏,产生靶向肿瘤外毒性。
痛点2:TME中低效应细胞浸润
在实体瘤中,T 细胞发挥功能首先需要渗透进入肿瘤内部。TME中实体瘤因稀疏甚至没有T细胞浸润,阻止了CD3-BsAbs将T细胞交联到肿瘤细胞,从而限制了治疗效果。
痛点3:免疫抑制TME
实体瘤的TME中的多种免疫抑制细胞类型会影响效应T细胞的质量。此外,免疫检查点会进一步降低肿瘤浸润淋巴细胞(TIL)的效应功能。
以上这些都是CD3-BsAbs现阶段在实体瘤领域所面临的挑战,要解决这些问题我们需要在这些领域找到CD3-BsAbs的有效性和安全性之间的平衡点,从而扩大CD3-BsAbs在实体瘤领域的治疗窗口。
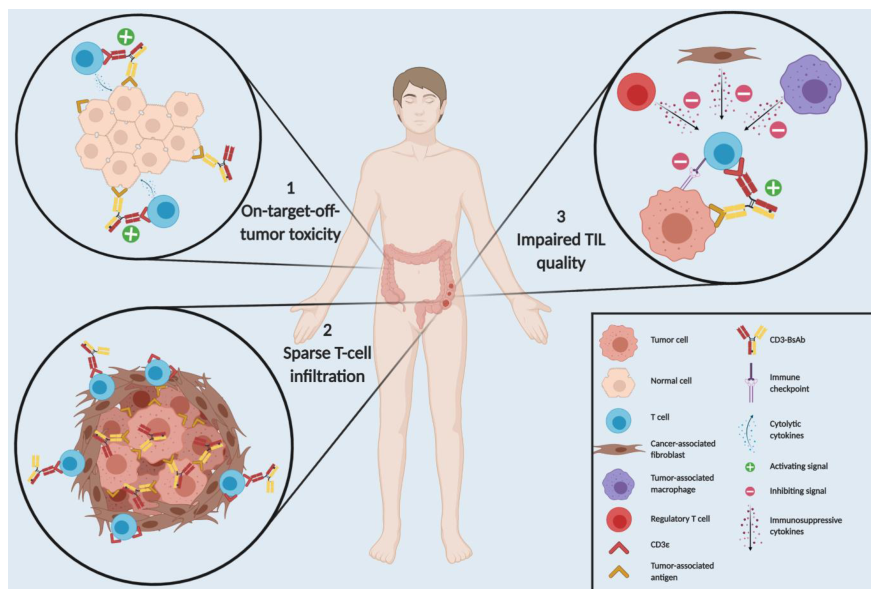
实体瘤CD3-BsAb治疗的三大障碍
【攻克】三大“黄金点”
黄金点1:毒性缓解
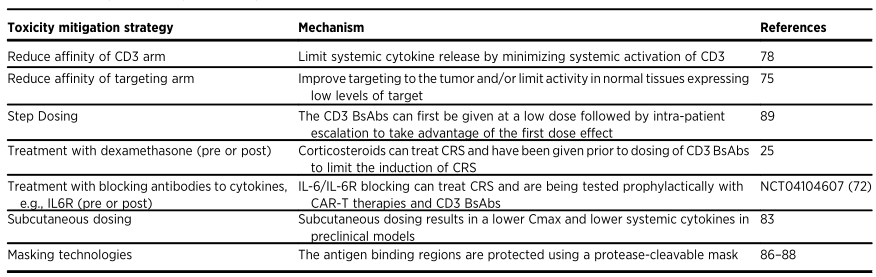
> 降低CD3亲和力:降低CD3亲和力可以维持抗肿瘤疗效,同时减少全身细胞因子的释放。
> 增加肿瘤特异性:增加肿瘤特异性的可以提高CD3-BsAbs靶向实体瘤的安全性。
> 阶梯给药/皮下给药...
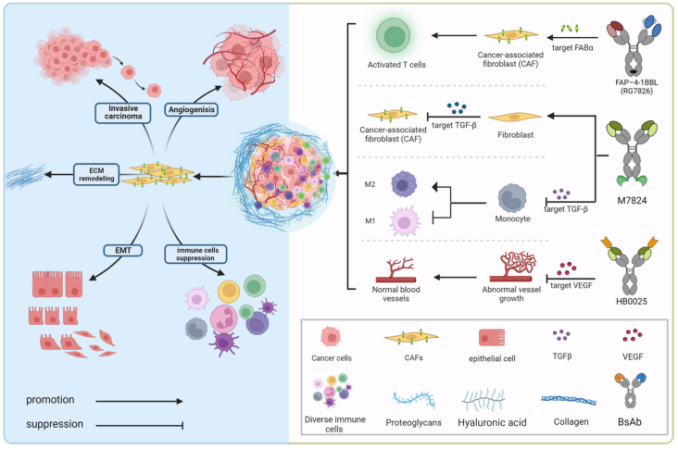
减轻CD3-BsAbs毒性的策略
黄金点2:免疫细胞浸润
> CD3-BsAbs联合:考虑到实体瘤内T细胞的衰竭及有限数量,CD3-BsAbs与其他疗法相结合或许可以强化反应效果。临床前研究表明,CD3-BsAbs联合治疗增加了肿瘤和免疫细胞上的PD-L1以及T细胞上的PD-1。
> 共刺激药物:共刺激信号可以增加T细胞扩增,从而增加效应T细胞的数量。临床前模型研究表明,当与CD3-BsAbs联用时,抗4-1BB延长了T细胞活化并增强了抗肿瘤功效。
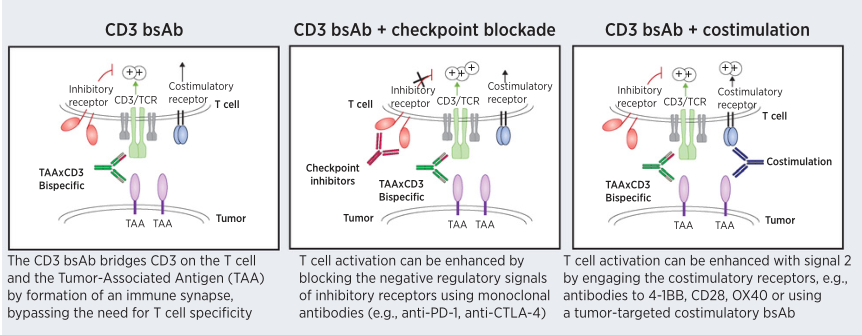
黄金点3:强化T细胞反应质量
> 削弱T细胞抑制信号:靶向免疫抑制细胞会耗尽免疫抑制细胞因子,从而降低T细胞的抑制信号,改善其效应器功能。
> 触发T细胞上的刺激性受体:CD3-BsAbs与共刺激抗体的组合已成功用于小鼠的多种肿瘤模型中。如:CD3xPSMA、双抗与共刺激激动剂4-1BB Ab的组合强化了抗肿瘤功效,提高了携带实体肿瘤小鼠的存活率。
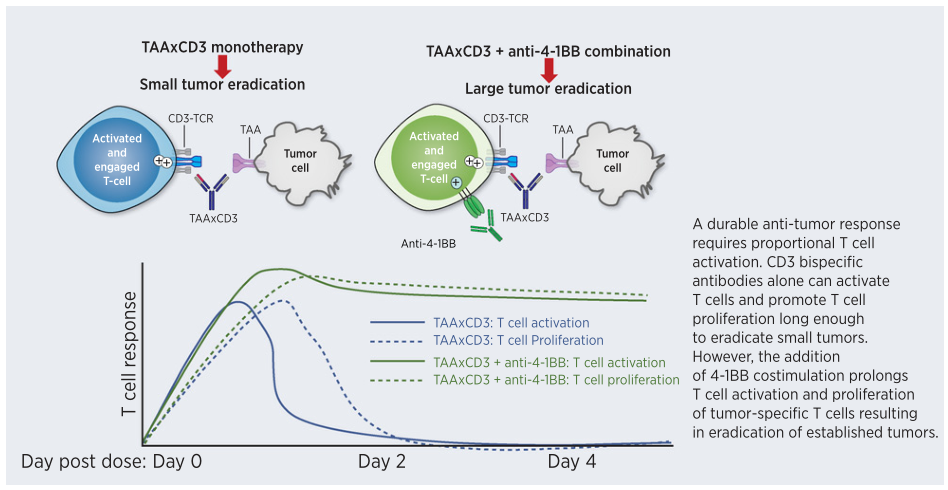
肿瘤根除与T细胞激活程度的相关性示意图
虽然CD3-BsAbs在实体瘤领域存在难点及痛点,但前述策略表明有很多前瞻性的策略组合方法可以形成突破,或为CD3-BsAbs在实体瘤治疗领域带来更多的可能。
ACROBiosystems百普赛斯优化开发了高度均一的高活性CD3δ/ CD3ε, CD3γ/ CD3ε系列产品,经非还原电泳和MALS技术严格确认为1:1异源二聚体,在抗体药物的开发和筛选、抗体药物的鉴定和质控、以及临床血药浓度分析等不同的应用技术平台中均表现出优异的性能,经双特异性临床抗体验证,符合药物开发要求,可加速双抗药物的开发进程。
| CD3E & CD3D | CD3 epsilon | CD3 gamma |
| CD3E & CD3G | CD3 delta |
点击图片查看更多双抗靶点蛋白
CD3系列蛋白—针对药物各应用场景开发
应用场景1:抗体药物开发和筛选
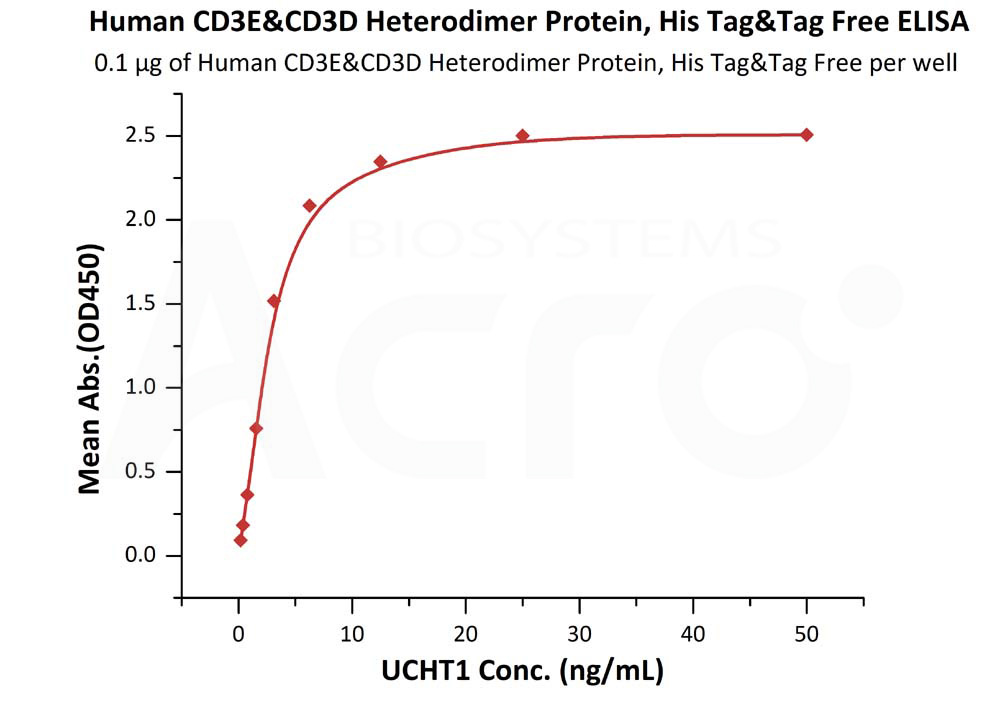
Immobilized Human CD3E&CD3D Heterodimer Protein, His Tag&Tag Free (Cat. No. CDD-H52W1) at 1 μg/mL (100 μL/well) can bind UCHT1 with a linear range of 0.2-6 ng/mL (Routinely tested).
应用场景2:抗体药物鉴定和质控
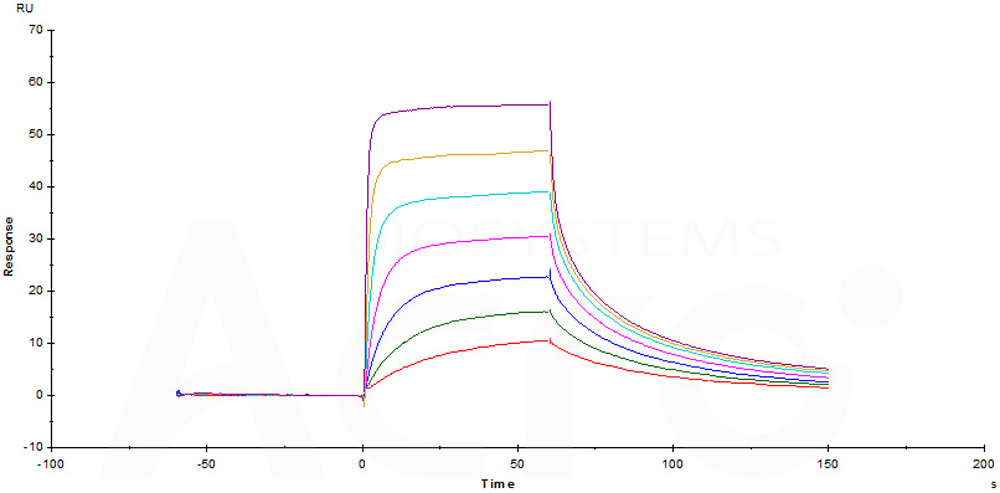
Biotinylated Human CD3E&CD3D Heterodimer Protein, His,Avitag&Tag Free (Cat. No. CDD-H82W6) captured on Biotin CAP - Series S sensor Chip can bind Anti-Human CD3 Antibody, Mouse IgG2a (Clone: OKT3) with an affinity constant of 22.5 nM as determined in a SPR assay (Biacore T200) (Routinely tested).
应用场景3:临床血药浓度分析
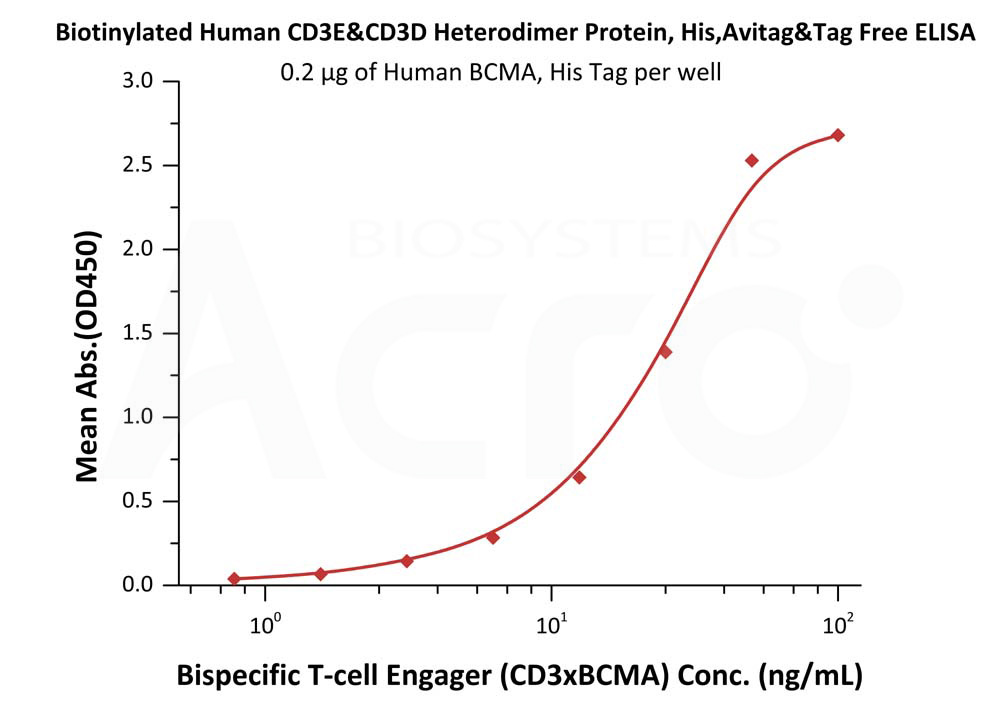
Immobilized Human BCMA, His Tag (Cat. No. BCA-H522y) at 2 μg/mL, add increasing concentrations of Bispecific T cell Engager (CD3 X BCMA) in 10% human serum and then add Biotinylated Human CD3E&CD3D Heterodimer Protein, His,Avitag&Tag Free (Cat. No. CDD-H82W6) at 0.2 μg/mL. Detection was performed using HRP-conjugated streptavidin with sensitivity of 15 ng/mL (Routinely tested).

ACROBiosystems
inquiry@acrobiosystems.com
15117918562
(备注:姓名+公司)
参考文献
1. Wei J, Yang Y, Wang G, et al. Current landscape and future directions of bispecific antibodies in cancer immunotherapy[J]. Frontiers in Immunology, 2022, 13: 6573.
2. Wang Y T, Ji W D, Jiao H M, et al. Targeting 4-1BB for tumor immunotherapy from bench to bedside[J]. Frontiers in Immunology, 2022, 13.
3. Crawford A, Chiu D. Targeting solid tumors using CD3 bispecific antibodies[J]. Molecular Cancer Therapeutics, 2021, 20(8): 1350-1358.
4. Middelburg J, Kemper K, Engelberts P, et al. Overcoming challenges for CD3-bispecific antibody therapy in solid tumors[J]. Cancers, 2021, 13(2): 287.
5. Chiu D, Tavaré R, Haber L, et al. A PSMA-Targeting CD3 Bispecific Antibody Induces Antitumor Responses that Are Enhanced by 4-1BB CostimulationEnhancing PSMAxCD3 Antitumor Efficacy with Costimulation[J]. Cancer Immunology Research, 2020, 8(5): 596-608.