2021年初,发表在《Nucleic Acids Research》上关于m5C的文章研究了NSUN6可做为m5C mRNA甲基化修饰酶,可能参与mRNA翻译过程。此外也有多篇文章报道了m5C在众多研究方向的机制。那么这个最新领域具体有哪些进展?有哪些新型的方法思路值得我们借鉴呢?小编汇集了近期m5C修饰文章,带大家把握这一领域的最新进展。
文章展示
1. m5C——NSUN6介导m5C mRNA甲基化修饰的序列和结构特异性
发表期刊:Nucleic Acids Research影响因子:11.501
文章链接:Sequence- and structure-specific cytosine-5 mRNA methylation by NSUN6
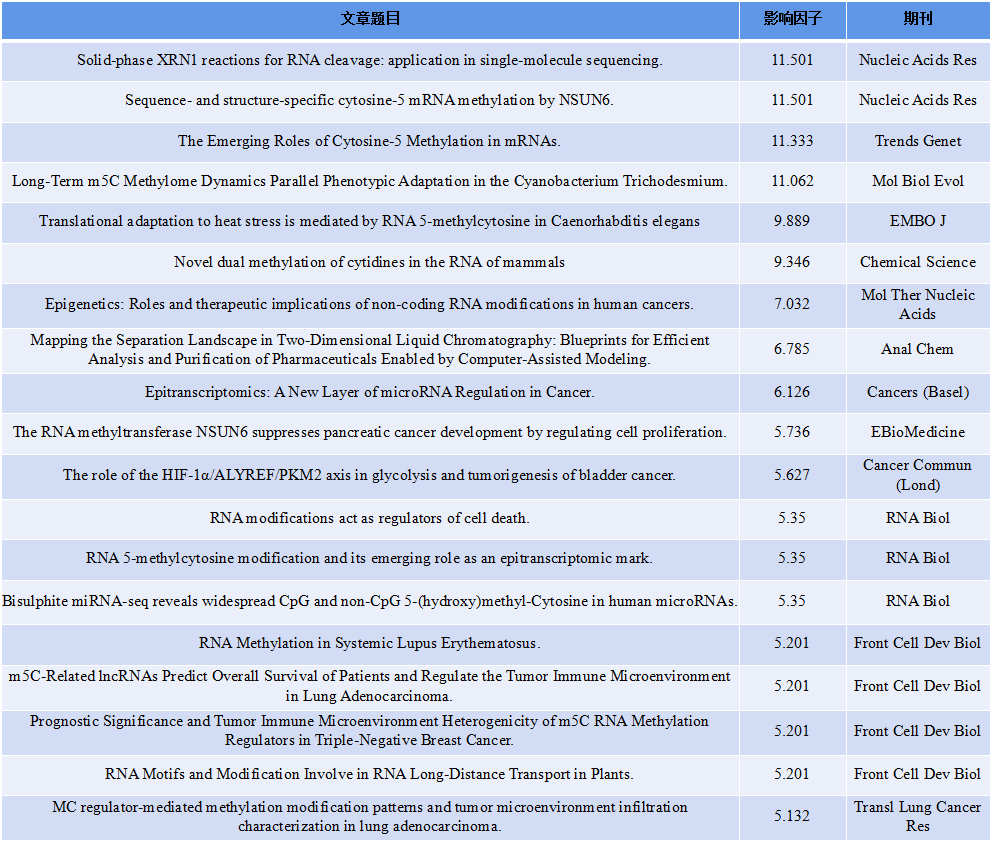
高丰度的m6A RNA修饰对mRNA功能具有十分重要调控作用,而m5C修饰的功能在很大程度上仍不为人知。本文中作者使用甲基化依赖的miCLIP技术结合RNA bis-seq测定了人类转录组中的m5C修饰位点。结果发现NSUN6是一种甲基转移酶,对mRNA具有很强的底物特异性。NSUN6主要作用于3’UTR区的保守基序CTCCA。敲除和回复实验显示,NSUN6靶向调控mRNA甲基化。核糖体分析进一步证明NSUN6特异性甲基化与翻译终止相关。虽然NSUN6在小鼠胚胎发育中是必不可少的,但它在人类肿瘤中表达下调,且NSUN6的高表达的某些癌症患者有更好的预后。总之,该研究确定NSUN6是靶向mRNA的m5C甲基转移酶,可能是参与翻译终止保真度的质量控制机制的一部分。
图例1:miCLIP检测m5C修饰位点。
2. m5C——m5C RNA修饰介导秀丽隐杆线虫中热胁迫的翻译适应性
发表期刊:EMBO J
影响因子:9.889
文章链接:Translational adaptation to heat stress is mediated by RNA 5-methylcytosine in Caenorhabditis elegans
m5C是RNA转录后的甲基化修饰,发现在生命中广泛存在。虽然已经对m5C-甲基转移酶进行了研究,但m5C修饰对整体的发育、稳态和应激的影响仍然未知。本研究中使用秀丽隐杆线虫生成了第一个RNA中没有m5C的生物体,证明了这种修饰是不必要的。作者测定了在体内RNA上的m5C位点定位和酶特异性,结果表明缺乏m5C修饰的动物对温度较为敏感。在分子水平上,作者发现m5C的缺失影响亮氨酸和脯氨酸的解码,从而降低富含这些氨基酸的转录本的翻译效率。最终发现亮氨酸UUG密码子的翻译受热激影响最大,说明m5C tRNA甲基化对热胁迫的适应过程起重要作用。
3. m5C——哺乳动物RNA胞苷的双甲基化研究
发表期刊:Chemical Science影响因子:9.346
文章链接:Novel dual methylation of cytidines in the RNA of mammals
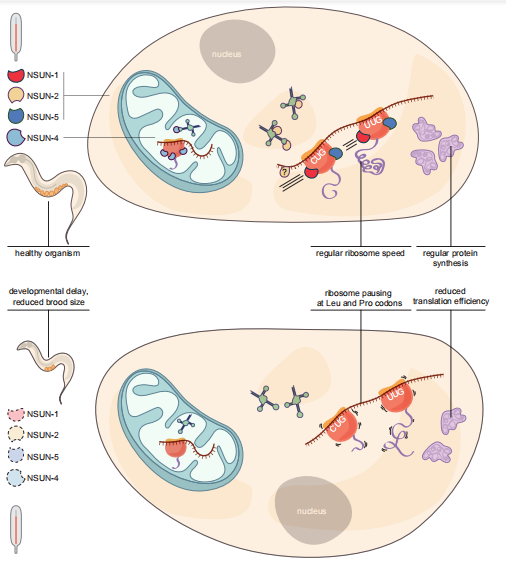
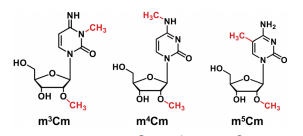
RNA修饰在调节各种生理过程中发挥着重要作用。甲基化是RNA中最普遍的修饰。在哺乳动物RNA中有三种同分异构体胞苷甲基化修饰,包括m3C、m4C、m5C。除了胞苷碱基上的单甲基化,也有报道在核糖的2’羟基和胞苷的碱基上n能发生双甲基化修饰,包括m4Cm和m5Cm。在大肠杆菌的16S rRNA中发现了m4Cm,而m5Cm在末端嗜热古菌和哺乳动物的tRNA中发现。但是,与m4Cm和m5Cm不同的是,推测的m3Cm双甲基化从未在生物体中被发现。因此,m3Cm在RNA中是否存在仍然是一个悬而未决的问题。在目前的研究中,作者合成了m3Cm,并建立了LC-ESI-MS/MS法测定胞苷二甲基化。在优化的分析条件下,m3Cm、m4Cm和m5Cm可以被清楚地分辨出来。利用该方法发现了m3Cm存在于哺乳动物RNA中。作者确认了m3Cm主要存在于哺乳动物小RNA (<200 nt)中。此外,作者第一次确认了m4Cm在哺乳动物细胞18S rRNA中的存在。同位素示踪表明,S -腺苷-L-蛋氨酸是RNA胞苷三种二甲基化的甲基供体。m3Cm的发现拓宽了生物体内RNA修饰的多样性。此外,m3Cm、m4Cm在哺乳动物中的发现为理解RNA修饰介导的RNA加工和基因表达调控开辟了新的方向。
4. m5C——RNA甲基转移酶NSUN6通过调节细胞增殖抑制胰腺癌的发生
发表期刊:EBioMedicine
影响因子:5.736
文章链接:The RNA methyltransferase NSUN6 suppresses pancreatic cancer development by regulating cell proliferation
胰腺癌(PC)由于其细胞过度增殖和侵袭性转移的特点成为世界上最致命的实体恶性肿瘤之一。有证据显示,RNA转录后修饰在PC进展中有重要作用。然而,关于PC中m5C RNA修饰的研究仍非常有限。在本研究中,作者采用定量PCR (qPCR)和免疫组化(IHC)方法检测362例正常人和382例肿瘤标本中与mvc相关的候选基因和蛋白表达情况。MTS法检测PC细胞增殖率。用异种移植小鼠模型来评估NSUN6在PC肿瘤形成中的作用。通过分析4个基因表达综合数据库(GEO),在3个独立的PC队列中选择了6个m5C相关基因,这些基因表现出显著且一致的变化,并进行进一步检查。最后,作者确定NSUN6的约简是所有PC样本集检测的共同特征。NSUN6表达与临床病理参数包括T分期和Ki67+细胞率相关。进一步评估50个PC组织的转录谱,发现在NSUN6低表达组中,细胞周期和G2M检查点等与细胞增殖相关的生物过程丰富。在体外PC细胞系和体内异种移植小鼠模型的帮助下,证实了NSUN6在调节细胞增殖和PC肿瘤生长中的作用。最后展示了NSUN6在评估PC患者肿瘤复发和生存率方面的良好表现。上述数据表明,NSUN6是调节PC细胞增殖的重要因素,并强调了基于mcc的新型临床模式作为PC患者治疗方法的潜力。
5. m5C——HIF-1α/ALYREF/PKM2调控通路在膀胱癌糖酵解和肿瘤发生中的作用
发表期刊:Cancer Communications
影响因子:5.627
文章链接:The role of the HIF-1α/ALYREF/PKM2 axis in glycolysis and tumorigenesis of bladder cancer
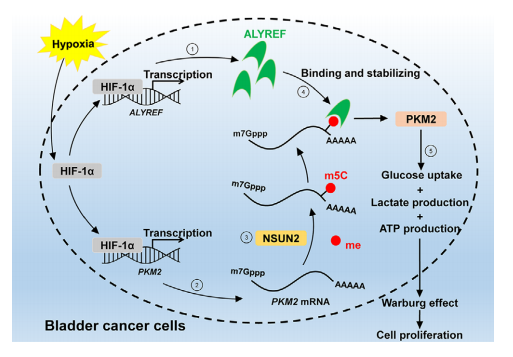
作为糖酵解的限速酶,丙酮酸激酶肌同工酶M2 (PKM2)参与肿瘤的代谢和生长。PKM2在肿瘤中的调控网络复杂,在膀胱癌中的研究尚不充分。研究发现PKM2 mRNA的m5C修饰可能参与了膀胱癌的发病机制。本研究首先证明了膀胱癌中ALYREF可稳定PKM2 mRNA并结合到其3'-UTR区的m5C位点。ALYREF的过表达可通过PKM2介导的糖酵解促进膀胱癌细胞增殖。此外,PKM2和ALYREF高表达预示膀胱癌患者生存期较差。最后,作者发现缺氧诱导因子-1α (HIF-1α)除了直接激活ALYREF的转录外,还通过激活其间接上调PKM2的表达。综上所述HIF-1α/ALYREF/PKM2轴中PKM2 mRNA的m5C修饰可能促进膀胱癌的糖代谢,为膀胱癌提供了一个新的有前景的治疗靶点。
云序生物m5C甲基化研究五大模块
m5C RNA甲基化测序(m5C-seq)
对m5C RNA甲基化,目前最流行的检测手段为m5C-Seq技术,适用于m5C RNA甲基化谱研究,快速筛选m5C RNA甲基化靶基因。云序可提供mRNA和多种非编码RNA的m5C测序:
- m5C 全转录组测序(涵盖mRNA,LncRNA,circRNA)
- m5C LncRNA测序(涵盖LncRNA和mRNA)
- m5C Pri-miRNA测序(涵盖Pri-miRNA和mRNA)
- m5C mRNA测序
LC-MS/MS检测整体RNA甲基化水平
精准高效,可以实现一次检测,9类修饰水平检测,一步到位。
03 m5C RNA甲基化上游酶的筛选
m5C RNA甲基化相关酶PCR芯片
寻找上游直接调控m5C RNA甲基化的甲基转移酶。
04 m5C RNA甲基化靶基因验证
meRIP-qPCR
云序提供各类不同修饰的meRIP-qPCR服务,可针对mRNA,lncRNA,环状RNA等不同类型的RNA分子进行检测,低通量验证RNA修饰靶基因表达水平。
05机制互作研究
5.1 RIP-seq/qPCR
筛选或验证RNA修饰直接靶点,研究RNA修饰靶基因的调控机制。
5.2 RNA pull down -MS/WB
筛选或验证目标RNA互作基因或蛋白,研究相应的分子调控机制。
5.3 双荧光素酶实验
验证两基因互作,研究相应的分子调控机制。
云序生物服务优势
优势二:至今完成4000+例 RNA甲基化测序样本,全面覆盖医口、农口等各类样本。
优势三:全面检测mRNA和各类非编码RNA(circRNA,lncRNA,Pri-miRNA等)。
优势四:独家提供m5C一站式服务:m5C整体水平检测、m5C测序、MeRIP-qPCR验证、RIP和RNA pull-down等。
优势五:率先研发超微量MeRIP测序技术,RNA量低至500ng起。
优势六:国内最全的RNA修饰测序平台,提供m6A、m6Am、m5C、m1A、m7G、m3C、O8G、ac4C乙酰化和2'-O-甲基化测序。
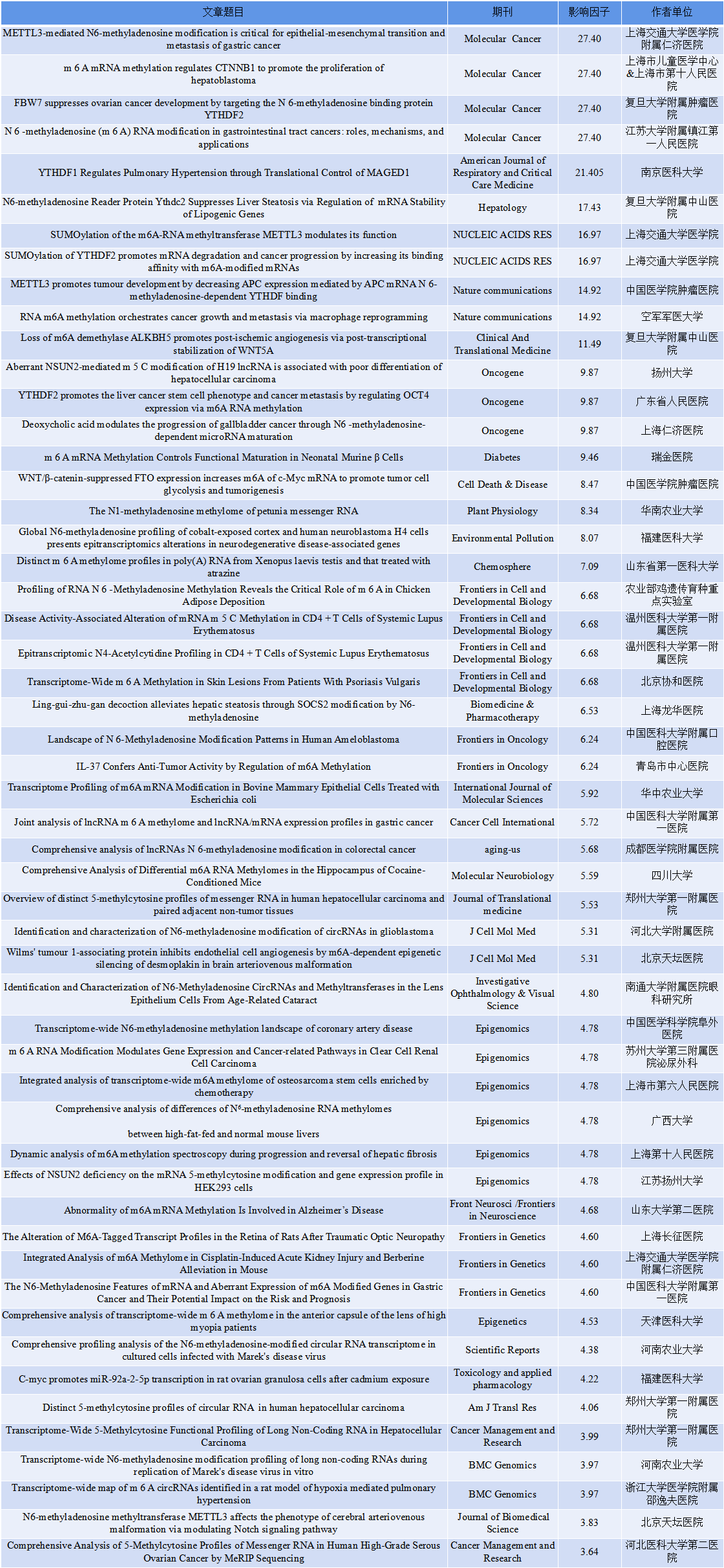
云序客户RNA修饰文章列表
相关产品
往期RNA修饰文章回顾
云序再推RNA修饰重磅新品:m6Am甲基化测序!
项目文章|赫捷院士团队nature子刊揭示METTL3以m6A依赖的方式调控食管鳞癌
经典思路|云序客户circRNA+m6A案例教您快速发表5分文章
m6A项目文章|ALKBH5通过调控WNT5A稳定性促进缺血后血管生成
云序客户再发15分文章:FBW7靶向m6A结合蛋白YTHDF2抑制卵巢癌
地 址: 上海市松江区莘砖公路518号24号楼4楼 联系人: 戴小姐 电 话: 021-64878766 传 真: 021-64878766 Email:market@cloud-seq.com.cn;liuqingqing@cloud-seq.com.cn
上海云序生物科技有限公司
商家主页
