促红细胞生成素(Erythropoietin,EPO)是一种在肾脏中主要产生的具有进化保守性的激素,EPO属于第一类细胞因子超家族,由165个氨基酸形成四个α螺旋结构(图1)。
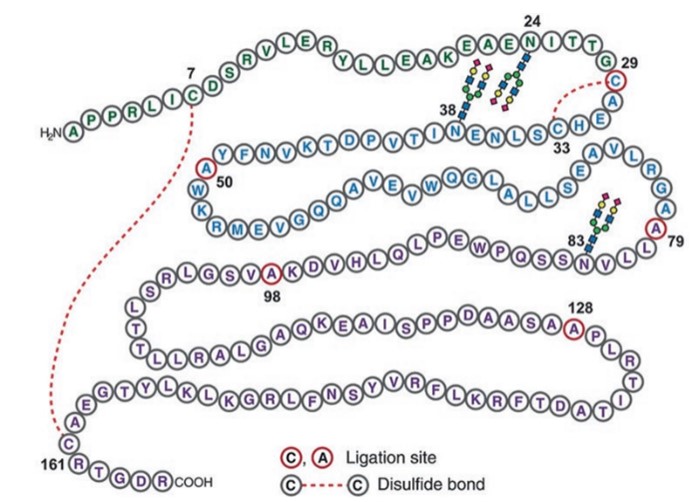
图1 人EPO的一级结构及其氨基酸序列
hEPO与LNPs-mRNA
mRNA药物作为一种新型的治疗手段,在疫苗、蛋白替代治疗,癌症免疫治疗,免疫细胞工程等方面具有广阔的应用前景,脂质体纳米粒(LNPs)作为修饰mRNA的主要递送工具,其递送效率直接影响mRNA药物的药效。
为评估LNPs的体外递送效率和mRNA药效,研究人员使用装载不同含量的修饰hEPO-mRNA的LNPs转染Huh7细胞,基于EPO是分泌蛋白,可以从细胞中分泌出来,因此,可在指定的时间点收集细胞上清,并使用ELISA来测定hEPO的表达,研究结果显示,在体外研究中,Huh7细胞以剂量依赖和时间依赖的方式能有效表达hEPO(图2)。
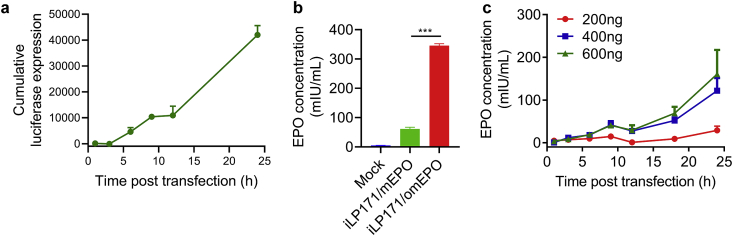
图2 iLP171/mRNA介导的体外蛋白质表达
同时,为评估LNPs的体内递送效率和mRNA药效,将装载修饰hEPO-mRNA的不同类型LNPs注射到小鼠体内,经过一段时间后,研究人员用ELISA方法检测小鼠血清中hEPO含量,来评估LNPs的体内递送效率和mRNA的药效(图3)。
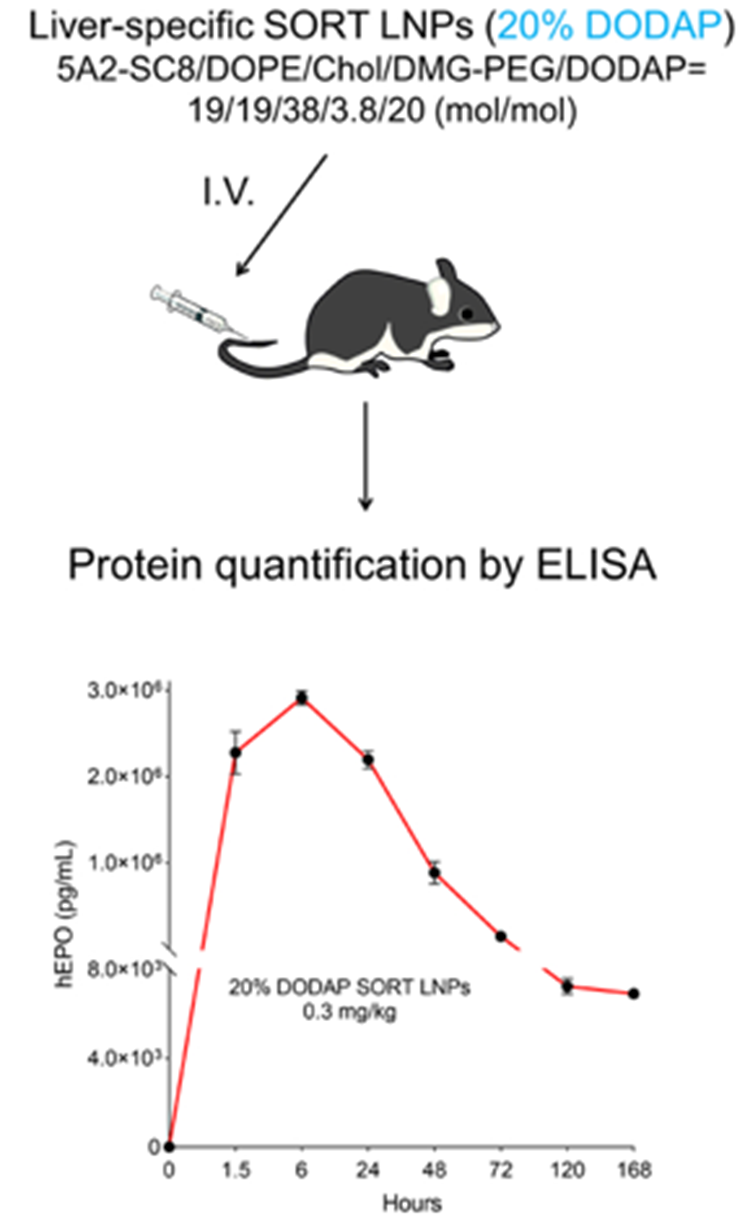
图3 分泌蛋白的mRNA递送方案
综上,通过ELISA技术检测细胞上清、血清中hEPO的含量,可有效地评估以脂质纳米粒子(LNPs)为基础的修饰mRNA的药理和药效相关研究。
为满足LNPs-mRNA药物研发中hEPO的检测需求,ACROBiosystems百普赛斯依托免疫分析平台开发了ClinMax™ Human Erythropoietin (EPO) ELISA Kit, PRO(货号:CEA-C027) ,具有更灵敏、检测速度更快等特性,满足多种复杂样本的检测需求,加速您的mRNA药物的开发进程。
ClinMax™ Human Erythropoietin (EPO) ELISA Kit, PRO
(Cat. No. CEA-C027)
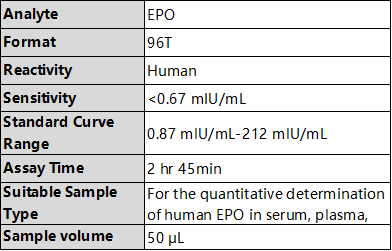
★ 更灵敏:定量下限0.87 mIU/mL;
★ 速度更快:采用一步法,3h内即可完成检测;
★ 经血清、血浆等真实样本检测,基质干扰小;
★ 遵循ISO9001和ISO13485双重质量体系,批间差异有保障;
★ 基于ACRO自主蛋白原料平台开发,产品性能、供货能力及长期稳定性保障;
★ 可提供方法学验证报告,严格控制产品灵敏度、特异性、准确度、线性和批间/批内差。
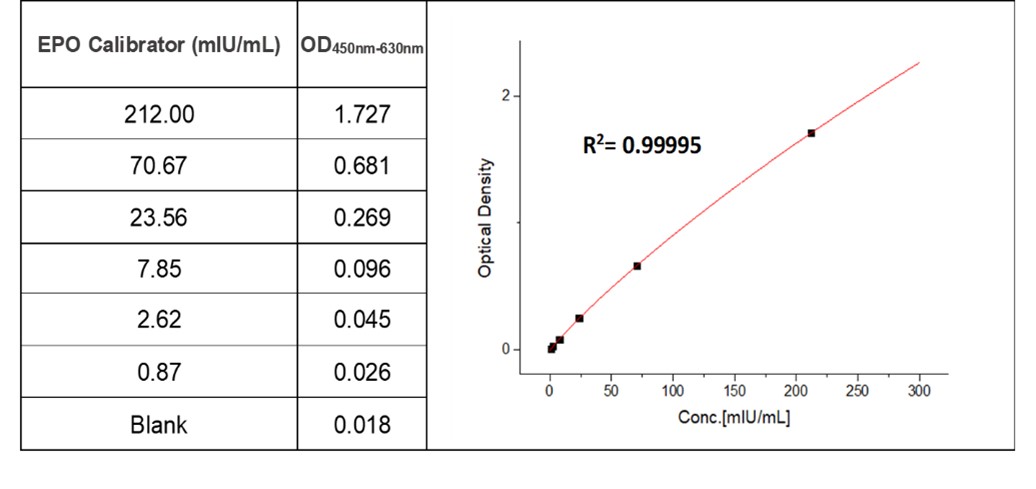
For each experiment, each ELISA plate needs to set the standard curve. The minimum detectable concentration of EPO is less than 0.67 mIU/mL.
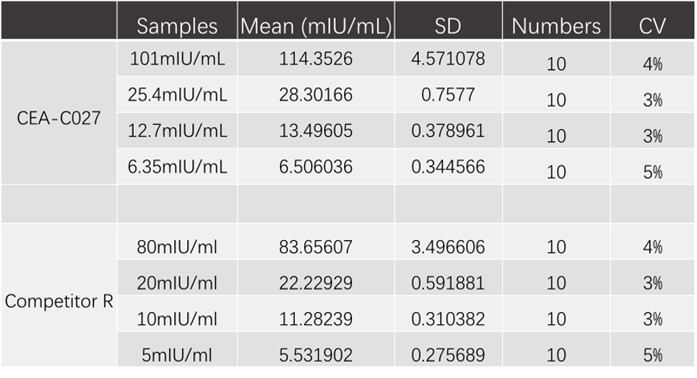
为评估CEA-C027和竞品R两个产品的精密度,测试了不同浓度的加标样本,每个浓度重复测试10次,可接受范围:CV< 10%。结果显示,所有样本的CV值都低于6%,优于接受范围。
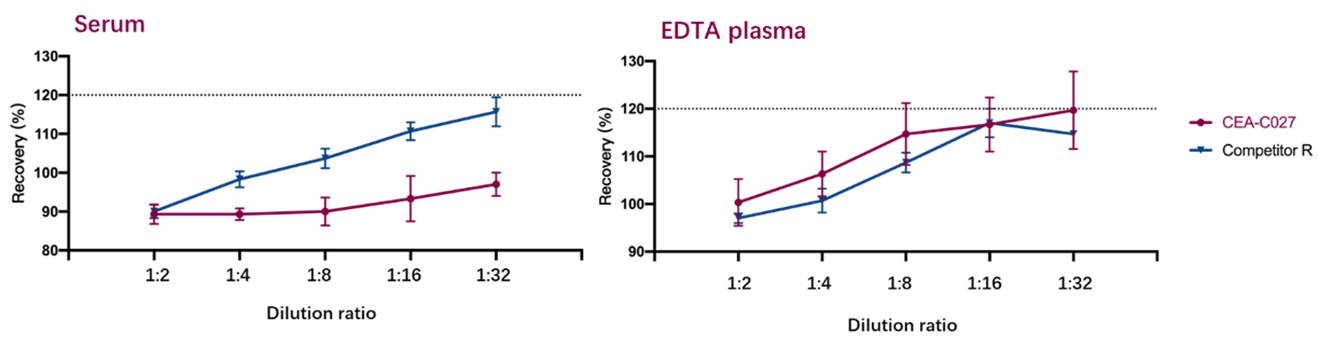
为评估CEA-C027和竞品R的稀释线性,对高值的加标样本(血清和EDTA血浆)梯度稀释后进行分析。结果显示,所有分析样本的平均回收率在90%-120%之间,在接受范围之内。
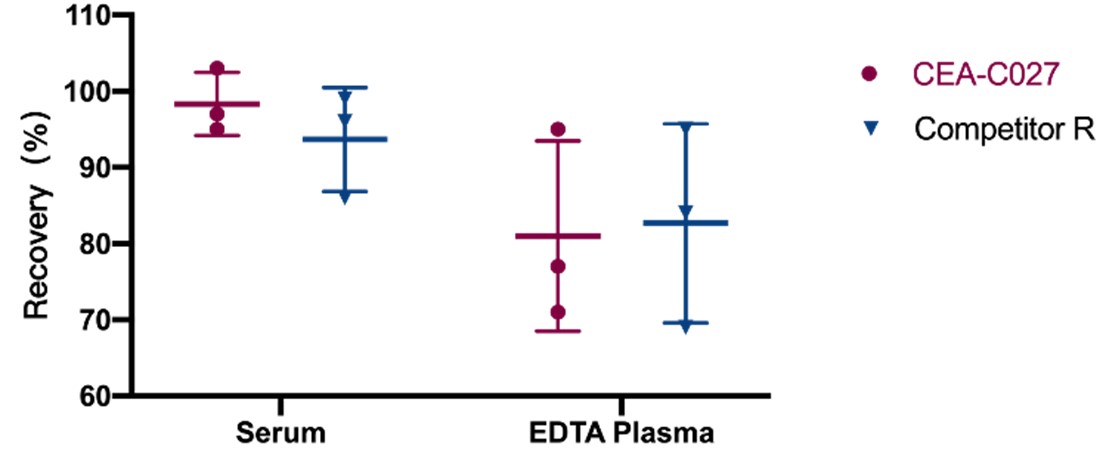
为评估CEA-C027和竞品R的回收率,对低值(加标量接近LLOQ)的加标样本(血清和EDTA血浆)进行分析。结果显示,血清和EDTA血浆样本的平均回收率在80%和110%之间。
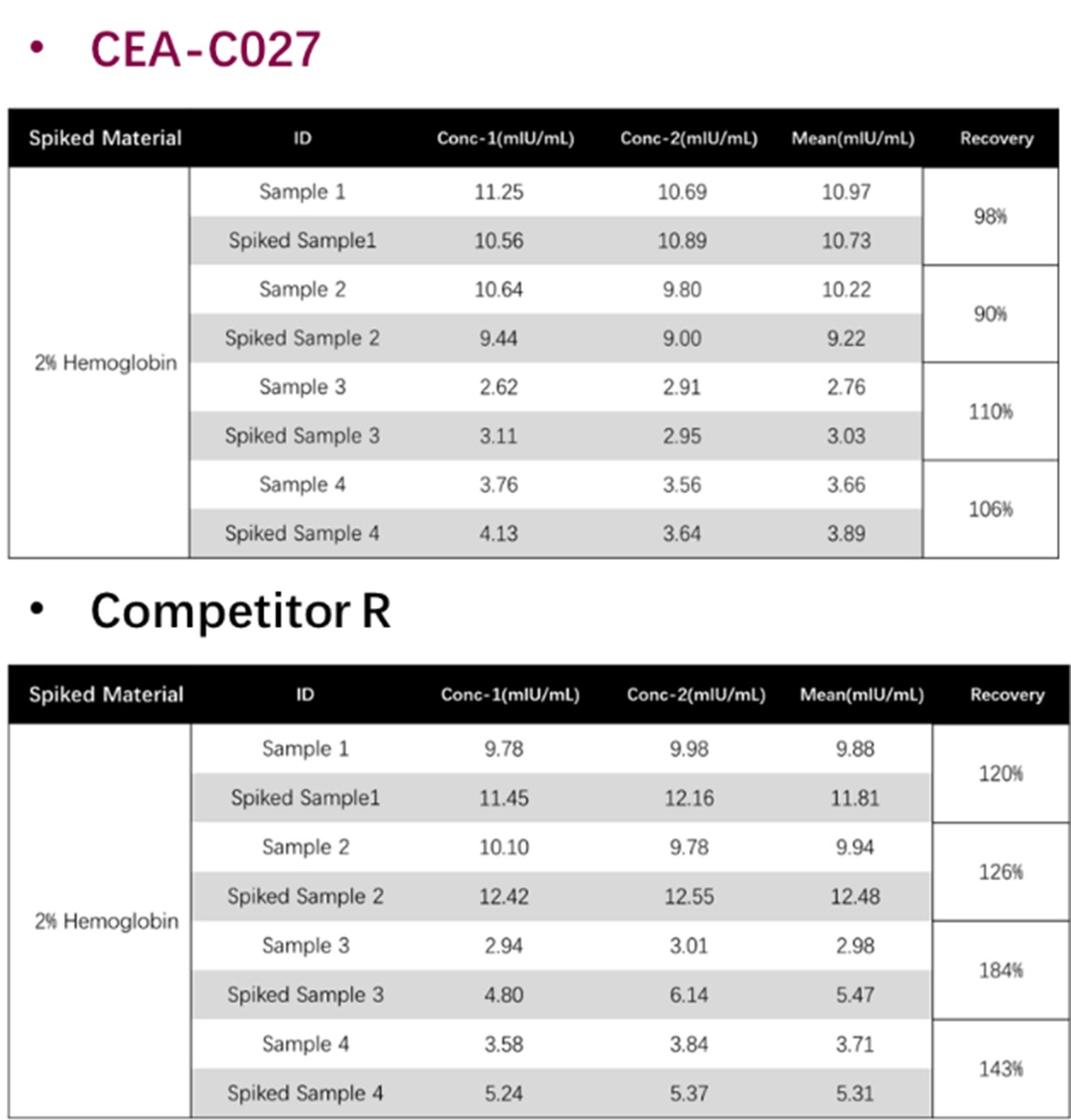
为了评估溶血对血清样本分析的影响,测试了2%血红蛋白的溶血模拟血清样本。结果显示,使用CEA-C027检测的分析物回收率在90%-110%之间,并没有受到溶血基质的影响,而溶血基质可能会影响竞品R的EPO检测。
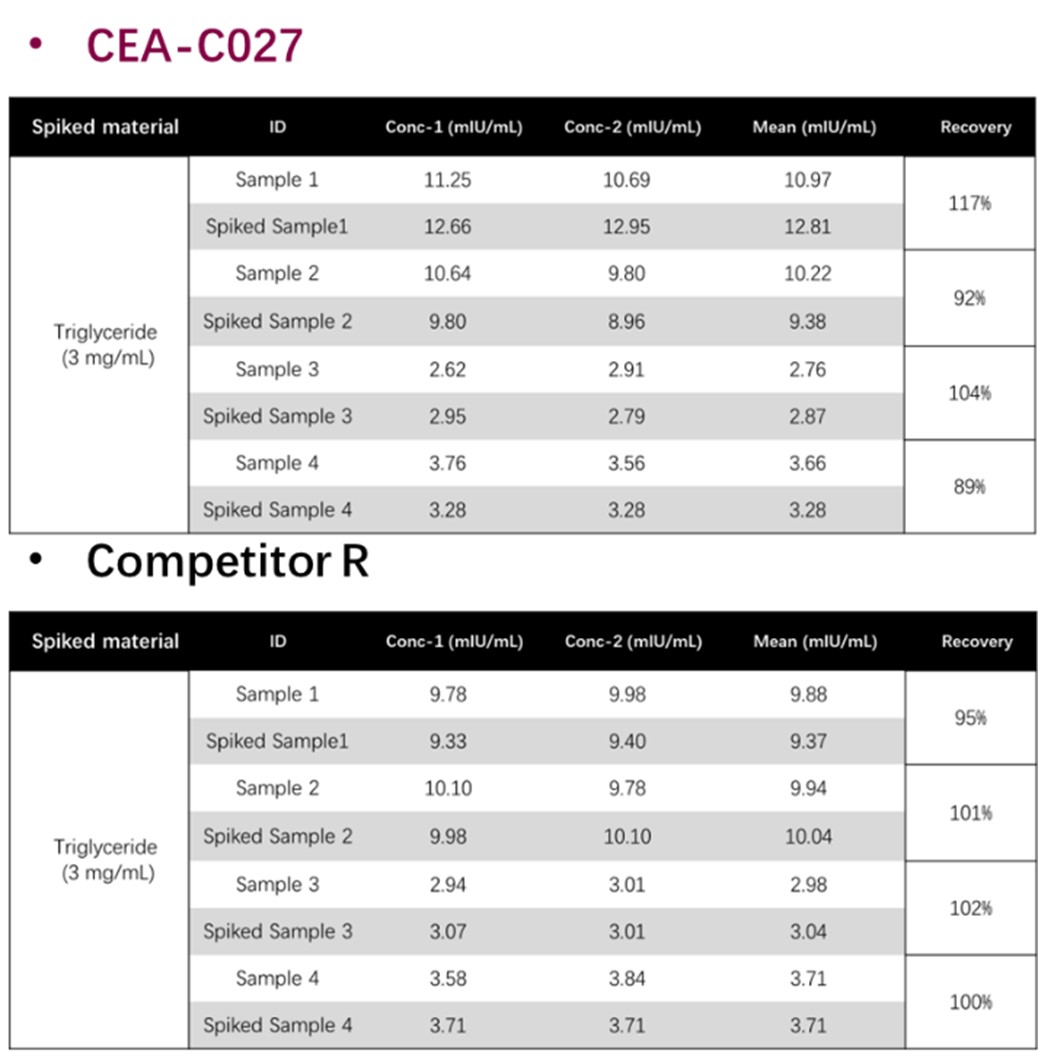
为了评估高脂对血清样本分析的影响,测试了3%甘油三酯的高脂模拟血清样本。结果显示,所有分析物回收率都在80%-120%之间,两个试剂盒都没有受到高脂基质的影响。
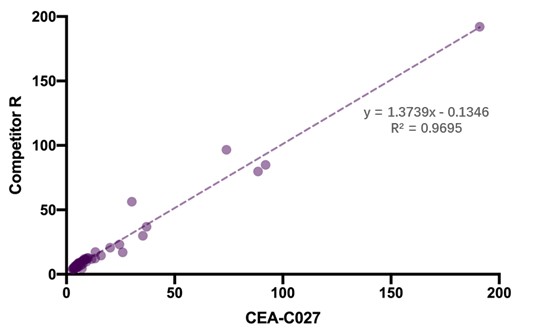
为了评估CEA-C027和竞品R的分析一致性,两个产品同时测试了40个健康人样本和14个病人样本。结果显示,两个产品检测结果的一致性高,R2>0.95。

ACROBiosystems
inquiry@acrobiosystems.com
15117918562
(备注:姓名+公司)
参考文献
1. https://link.springer.com/chapter/10.1007/978-3-030-35582-1_2
2. Yang T, Li C, Wang X, et al. Efficient hepatic delivery and protein expression enabled by optimized mRNA and ionizable lipid nanoparticle. Bioact Mater. 2020;5(4):1053-1061. Published 2020 Jul 13.
3. Cheng, Qiang et al. Selective organ targeting (SORT) nanoparticles for tissue-specific mRNA delivery and CRISPR-Cas gene editing. Nature nanotechnology vol. 15,4 (2020): 313-320.

