发表期刊:Advanced Science,IF=16.806
合作单位:上海交通大学附属第六人民医院
合作项目:胆汁酸与支链氨基酸靶向定量
研究介绍
2型糖尿病(T2D)患者体型一定是肥胖吗?当然不一定!体重正常甚至消瘦人士也可能被T2D盯上。此前有研究报道T2D和肥胖患者的肠道菌群发生改变,并且这些改变对疾病的发生和发展发挥重要作用,然而消瘦型T2D患者的肠道菌群的变化及其在这类疾病中的作用尚未阐明。上海交通大学附属第六人民医院贾伟平教授、李华婷研究员等团队在《Advanced Science》上发表研究成果,通过比较分析有无T2D的瘦或肥胖人群的肠道菌群结构与代谢特征,并联合小鼠模型验证,结果显示,消瘦型T2D患者AKK菌丰度减少,AKK菌的丰度与3β-鹅去氧胆酸(β-CDCA)水平呈负相关,并且该菌的减少与胰岛素分泌和葡萄糖稳态损害有关。这些结果为糖尿病的预防和精准治疗提供了重要的理论依据。
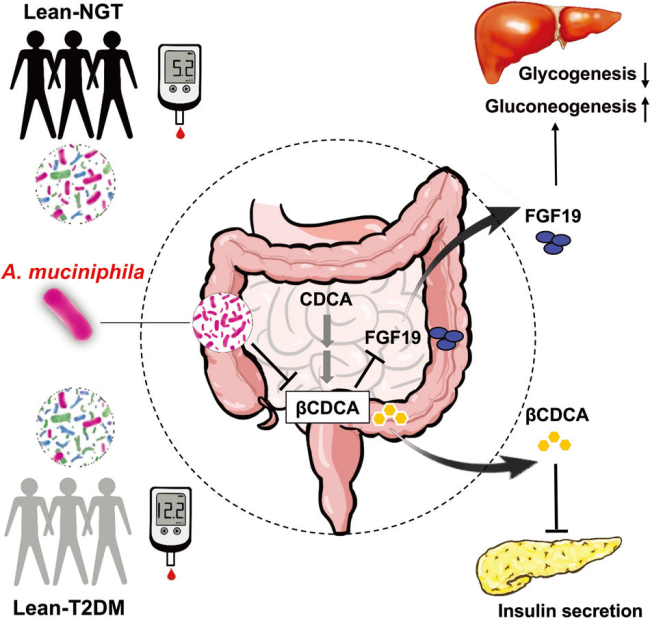
图1丨A. muciniphila对葡萄糖代谢的作用机制
研究思路
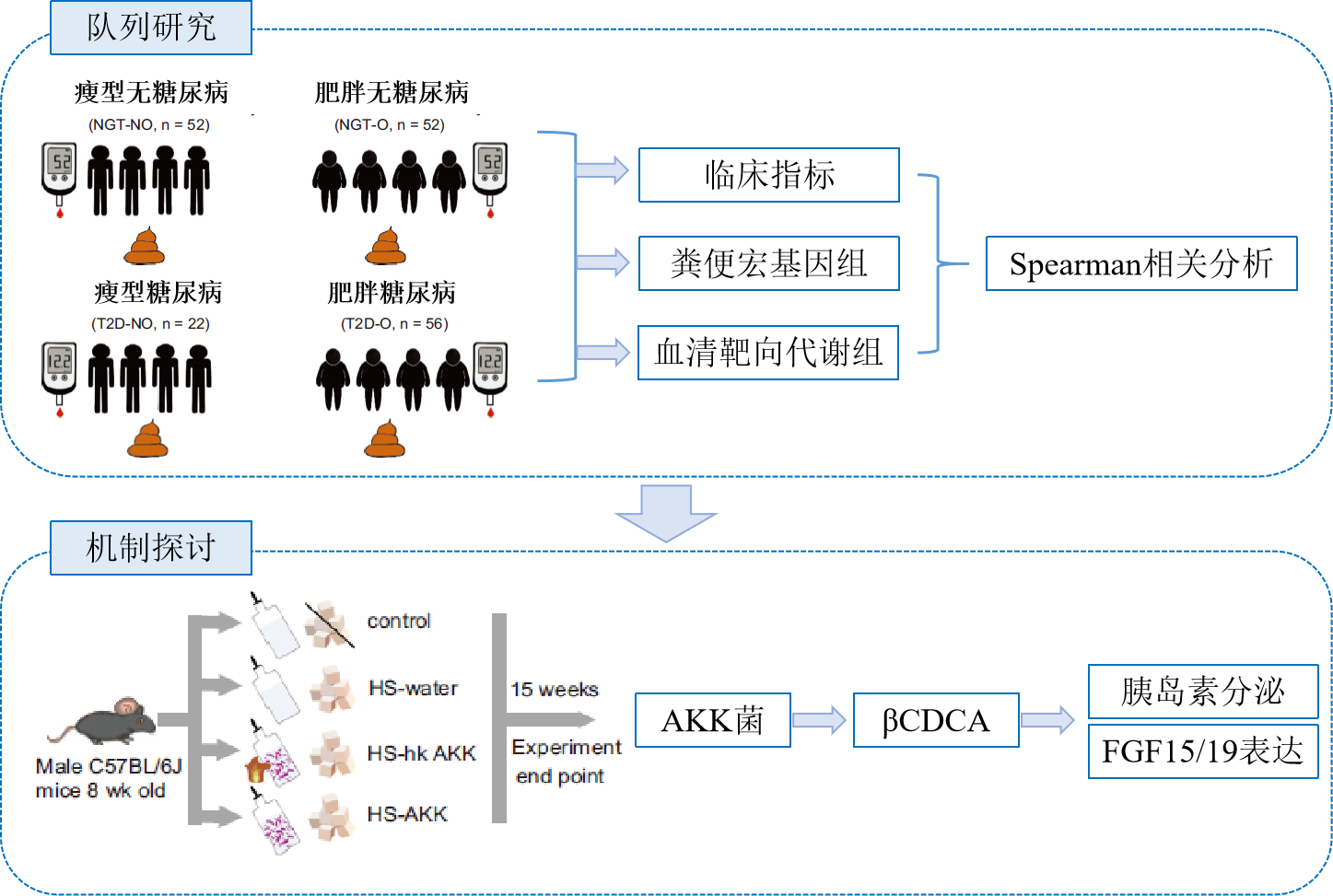
研究结果
1. 粪便宏基因组测序分析
纳入182名受试者,分为瘦型无糖尿病(NGT-NO)、腹部肥胖无糖尿病(NGT-O)、瘦型糖尿病(T2D-NO)和腹部肥胖糖尿病(T2D-O)四组。首先分析所有受试者临床数据,然后进行粪便宏基因组测序。结果显示,T2D-NO组α多样性高于T2D-O组,相较于其他三组,T2D-NO组菌群丰度分布是独特的。进一步分析两两组差异物种,发现T2D-NO 和 NGT-NO 组的特征在于某些特定物种,而不是整个群落的巨大变化。随后对四组人群微生物功能进行分析,结果显示T2D-NO组的菌群可能具有较低的碳水化合物利用能力和较高的支链氨基酸(BCAAs)产生能力。此外,与NGT-NO 组相比,参与碳水化合物代谢(包括“半乳糖降解”)模块在 T2D-NO组中高度富集。此外,研究人员发现一个标志菌种Akkermansia muciniphila,据报道,A. muciniphila是一种可以缓解肥胖的益生菌,本研究中T2D-NO组该菌丰度显著低于NGT-NO 组,而肥胖两组中没有显著差异,并且,A. muciniphila与胰岛素分泌呈正相关。
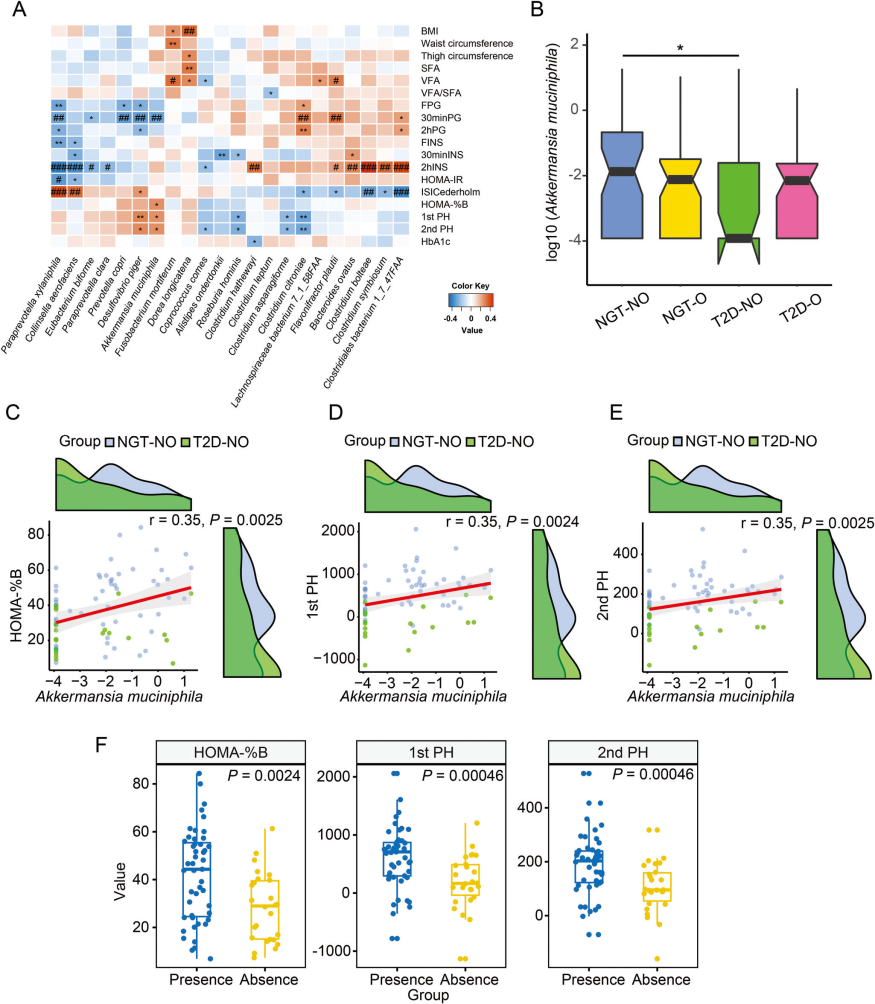
图2丨A. muciniphila与胰岛素分泌呈正相关
2. 血浆靶向代谢组学检测与相关性分析
肠道菌群的扰动可能会影响胆汁酸(BA)池的大小和组成,而血浆BAs的改变与代谢紊乱有关。每组筛选20名受试者进行胆汁酸谱检测,发现T2D-NO和NGT-NO组间有5个BAs差异显著,即甘氨酸熊去氧胆酸(GUDCA)、3β-鹅去氧胆酸(βCDCA)、β-熊胆酸(βUCA)、3β-胆酸(βCA)和熊胆酸(UCA)。对T2D-NO和NGT-NO组间的临床指标、BAs和肠道菌群进行相关性分析,结果显示,βCDCA与A. muciniphila和胰岛素分泌呈负相关,参与胆汁酸合成相关酶(baiB)与A. muciniphila呈正相关,与βCDCA呈负相关。总之,T2D-NO组A. muciniphila和baiB丰度降低,胰岛素分泌减少,βCDCA升高,提示A. muciniphila和胰岛素分泌可能由βCDCA介导的。
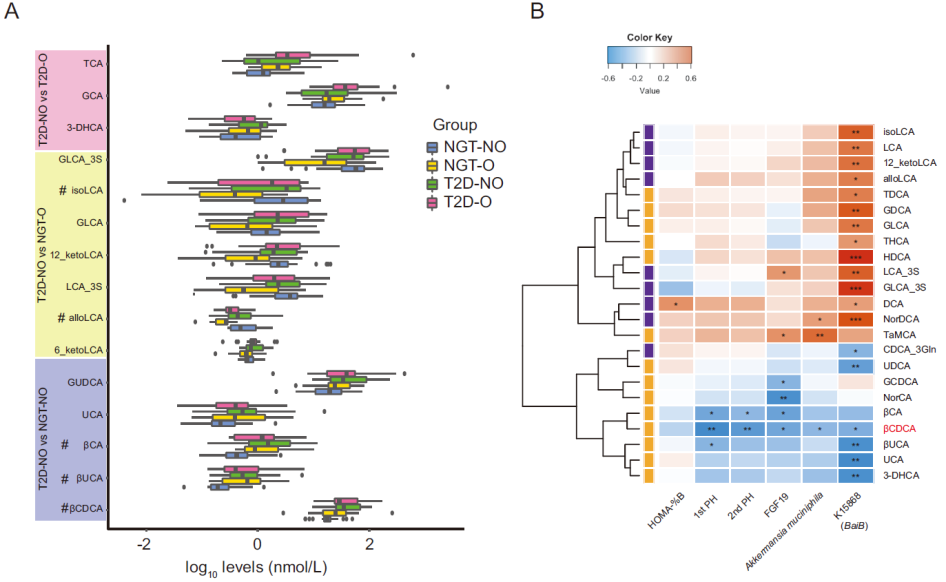
图3丨A. muciniphila与胆汁酸和FGF19的关系
3. A. muciniphila调控胰岛素分泌
利用高蔗糖(HS)饮食构建T2D-NO小鼠模型,分别添加水(HS-water)、A. muciniphila(HS-AKK)和高温杀死的A. muciniphila(HS-hk AKK),对照组(CON)正常饮食和高压灭菌水,喂养15周后比较四组小鼠体重、葡萄糖耐受和胰岛素分泌等,并进一步开展体内和体外试验。结果表明胰岛素分泌明显受损而非胰岛素抵抗的小鼠模型中A. muciniphila数量减少,通过补充活的A. muciniphila能够恢复胰岛素分泌并改善葡萄糖耐受。
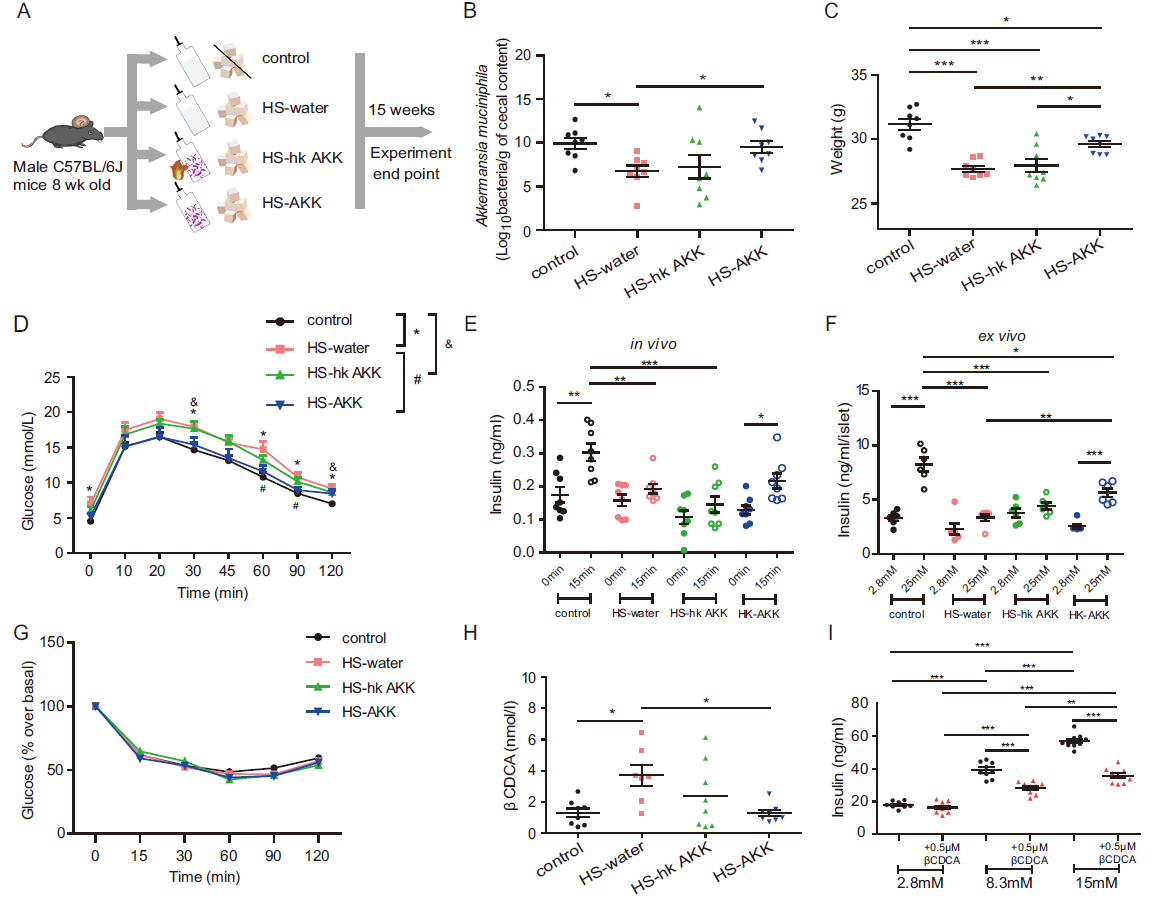
图4丨A. muciniphila对宿主代谢的作用
随后,对小鼠血清进行胆汁酸谱检测,发现活的 A. muciniphila 干预显著降低βCDCA 水平,而使用灭活的A. muciniphila不能导致βCDCA 显著降低,表明A. muciniphila可能通过降低肠道中βCDCA来刺激胰岛素分泌。
FGF19已被证明通过胰岛素独立途径刺激糖原合成并抑制糖异生。临床分析显示,与NGT-NO组相比,T2D-NO组血清FGF19水平显著降低。FGF19水平与A. muciniphila丰度呈正相关,与βCDCA水平呈负相关。为进一步探讨βCDCA能否抑制FGF15/19表达,研究人员在CDCA存在的情况下,用不同浓度的βCDCA培养人结肠上皮细胞LS174T,结果发现,CDCA联合βCDCA处理LS174T细胞可导致FGF19 mRNA表达水平呈剂量依赖性下降,提示βCDCA对肠道FGF15/19表达有抑制作用。因此,A. muciniphila可能通过限制βCDCA的可用性,增强FGF15/19的表达,进而刺激糖原合成,抑制糖异生。
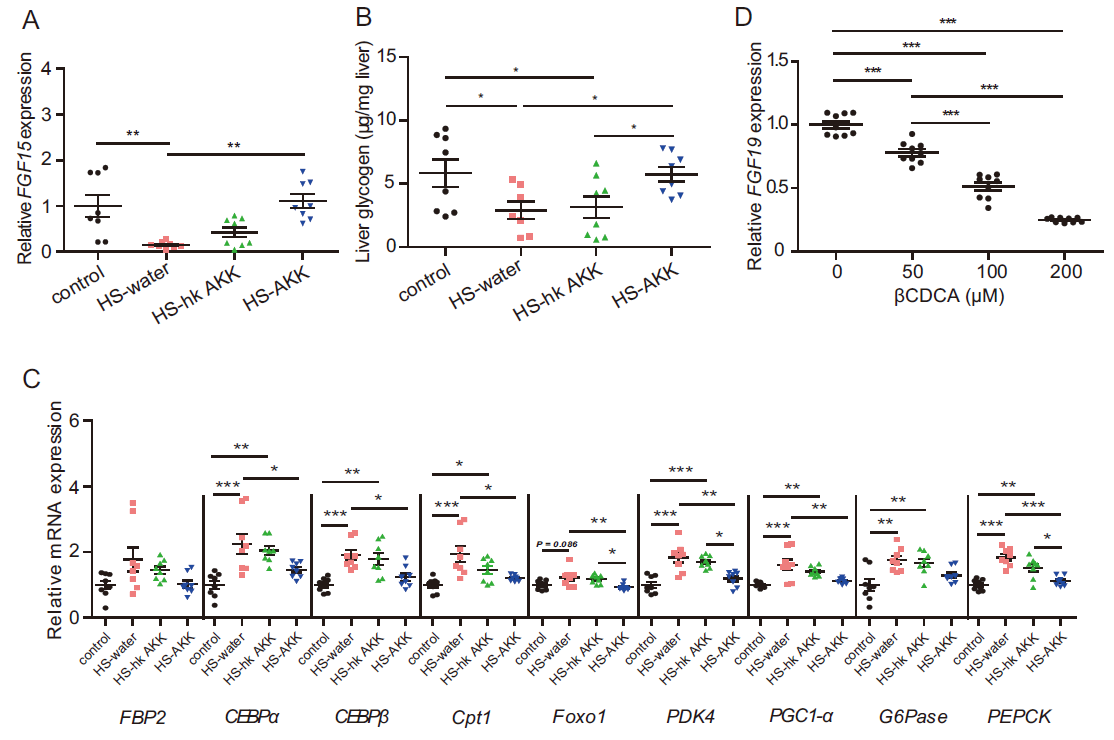
图5丨A. muciniphila对FGF15/19表达的作用
参考文献
Decreased Abundance of Akkermansia muciniphila Leads to the Impairment of Insulin Secretion and Glucose Homeostasis in Lean Type 2 Diabetes. Advanced Science. 2021.
原文阅读,请长按识别下方二维码

绘谱帮你测
通过代谢组学和宏基因组测序的结合,本研究阐明了AKK菌丰度减少诱导瘦型T2D的机制。该菌通过降低βCDCA,一方面促进胰岛素分泌,另一方面增强FGF15/19表达,促进糖原合成,抑制糖异生,从而为糖尿病的预防和精准治疗提供重要的理论依据。其中胆汁酸谱和支链氨基酸均由麦特绘谱提供检测。麦特绘谱拥有成熟的代谢组学检测平台,菌群16S测序和宏基因组等技术,以及联合分析等全套解决方案。独家的检测技术、全面的数据报告以及专业的售后探讨,助力您的科研探索之路不断创新和突破。欢迎联系麦特绘谱咨询热线400-867-2686获取详细资料!
往期回顾
1. 绘谱学堂 | 肠道菌群参与瘦型糖尿病胰岛素分泌和糖稳态调节新机制
2. 客户案例︱中药篇(一):二陈汤改善糖尿病大鼠的肠道菌群和脂质代谢紊乱
3. 好文双发 | 《Diabetes Care》&《BMC Medicine》:2型糖尿病肠道菌群特征如何调控?多吃水果!
4. Cell Host & Microbe | 石胆酸通过重塑肠肝轴改善减肥手术后糖尿病
5. 客户案例 | 粪菌移植影响肥胖大鼠对2型糖尿病的易感性

