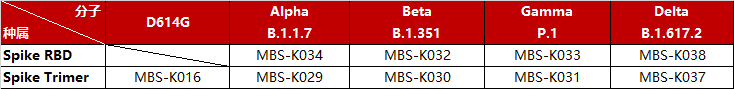
近期由于新冠病毒Delta突变株在印度、美国、英国、俄罗斯等地区快速传播,全球新冠疫情形势再次恶化,许多国家的每日新增确诊病例都创下历史新高,并且出现了“突破性感染”的病例。所谓“突破性感染”是指个体在全程接种完疫苗后仍然感染新冠肺炎的现象,即病毒突破了疫苗的防线,造成这种现象的原因之一是患者感染了部分或完全绕过疫苗保护的突变毒株。

大多数发挥中和作用的抗体靶向Spike RBD
首先,为了证实大多数发挥中和作用的抗体是靶向Spike RBD区域的抗体,这项研究选用了在不同时间点(症状消失后15-121天)采集的来自17个康复病人的35份血清样本,用偶联RBD的磁珠捕获并去除血清中的RBD抗体。研究人员用磁珠法处理前后的血清与Spike RBD或整个Spike胞外域蛋白分别进行ELISA结合实验,从而比较RBD抗体剥离前后的血清中和能力。实验表明,用磁珠法捕获RBD抗体可以有效去除血清中的RBD抗体,同时保留靶向其它结合位点的抗体。如图1所示,在分离血清中的RBD抗体后,血清与RBD的结合急剧减少,几乎完全消失;但与Spike的结合只减少了一些,说明血清中还有其它抗体存在。这项实验也向我们展示了RBD抗体在血清中总抗占有相当的比例。
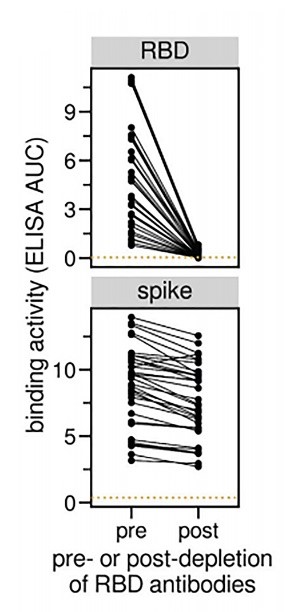
图1. 磁珠法分离RBD抗体前后(pre vs. post)康复血清对RBD(上)和spike(下)的结合活性。
同时,研究组测试了这35份血清样本在RBD抗体剥离前后对Spike (D614G) 假病毒的中和活性。结果显示,在约94%的样本中,血清的大部分中和活性是由RBD抗体提供的;在超1/3的样本中,RBD抗体提供了>90%的血清中和活性(图2)。通过磁珠和假病毒的方法,RBD抗体的关键作用得到验证,因此接下来的研究也聚焦在RBD上的突变。
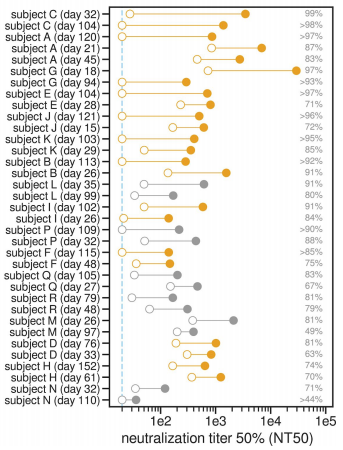
图2. 磁珠法分离RBD抗体前后(pre vs. post)35份康复血清对Spike(D614G)假病毒的中和抗体滴度(NT50)。实心球代表抗体分离前;空心球代表抗体分离后;标黄代表在后续实验中用于绘制突变逃逸图谱的血清样本。右侧的百分比数字代表血清总抗中由RBD抗体提供的中和活性。
“逃逸图谱”揭示导致中和下降的RBD突变
为全面分析所有可能导致抗体中和作用下降的RBD突变,该研究组通过deep-mutational scanning绘制出了RBD的突变图谱。该方法是通过建立一个庞大的酵母展示库,在每个酵母菌表面展示一种不同的RBD突变蛋白。整个文库包括了几乎所有可能发生的RBD单点突变。这项实验使用了康复后15-61天内收集的11份来自不同个体的血清样本。经D614G假病毒体系验证,这些选取的血清样本对RBD都有一定中和作用,其中RBD抗体为总抗提供的中和活性约为63-99%。实验将酵母展示库和康复血清一起孵育反应,然后利用荧光激活流式细胞术(FACS)分选并扩增对中和抗体作用呈现显著逃逸的RBD突变;并用deep sequencing技术测定某个特定RBD突变在新冠基因组中出现的频率。
研究组将每个RBD突变对血清中和作用的影响定义为该突变的“逃逸系数(escape fraction)”,这个系数越高,逃逸现象越明显;由此绘制出的“逃逸图谱(escape maps)”呈现出不同RBD突变的逃逸系数分布情况。研究组将逃逸系数高的RBD突变进行了分析和归类,发现它们可以被主要划分为三段突出的RBD结合位点(图3):1. Receptor-binding motif(RBM)上的一段receptor-binding ridge;2. 443-450 loop;3. core RBD epitope。RBM上的突变包括E484及发生在E484附近的L455,F456,G485,F486,F490等。据报道,有很多中和活性强的中和抗体靶向443-450这一区间,包括Regeneron鸡尾酒疗法中的两种抗体。Core RBD位于距RBM稍远的位置,靶向这一区域的抗体普遍活性不强,和SARS存在交叉。
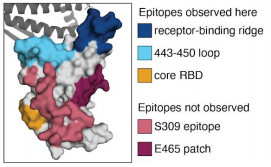
图3. 重要RBD突变位点区间划分
面对突变,康复者免疫防线变化如何?
为探究康复者如果二次暴露在突变病毒的风险下,免疫防线将受到怎样的影响,研究组对血清抗体活性随时间的变化做了进一步实验。他们在稍晚的时间点(康复后76-121天)再次采集了以上11个康复病人的血清,重复实验并绘制了逃逸图谱。结果显示,在超半数样本中,血清和突变RBD的结合活性无明显变化,说明血清抗体的特异性保持不变;但在少数样本中,血清随着时间过去变得更加广谱,能够结合更多突变RBD;在一例样本中,F456和E484突变对血清活性的影响在初期不明显,但在后期显现出来。因为样本量较少,无法得出明确结论,但可以看出病毒突变对中和抗体免疫防线的弱化作用随个体和时间不同而变化;且有些血清型对突变有更强的抵抗力。
在大多数情况下,导致抗体结合降低的RBD突变也会降低抗体中和活性,这一点通过spike假病毒中和实验得到了验证。使中和作用产生最显著下降的突变是E484(10-60倍),G446(30倍),G485(3-5倍)等(图4)。在某些样本中,血清中和抗体对E484K/E484Q/E484P的中和活性下降可以达到35-60倍;而10倍左右的下降即相当于去除所有血清中RBD抗体的活性损失。
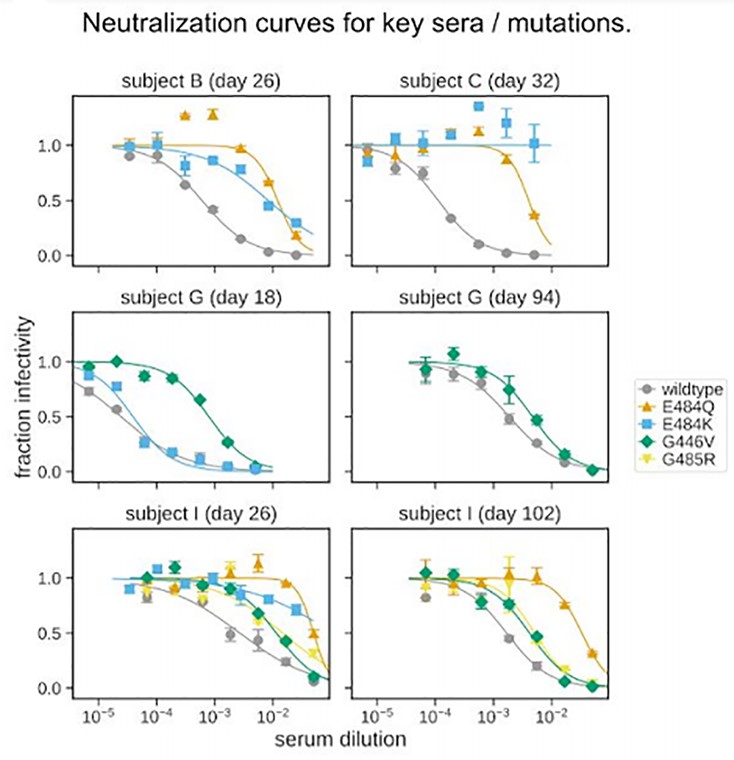
图4. 假病毒中和实验验证不同血清型对不同spike突变的中和作用
上述RBD免疫逃逸位点是否在真实世界中存在?
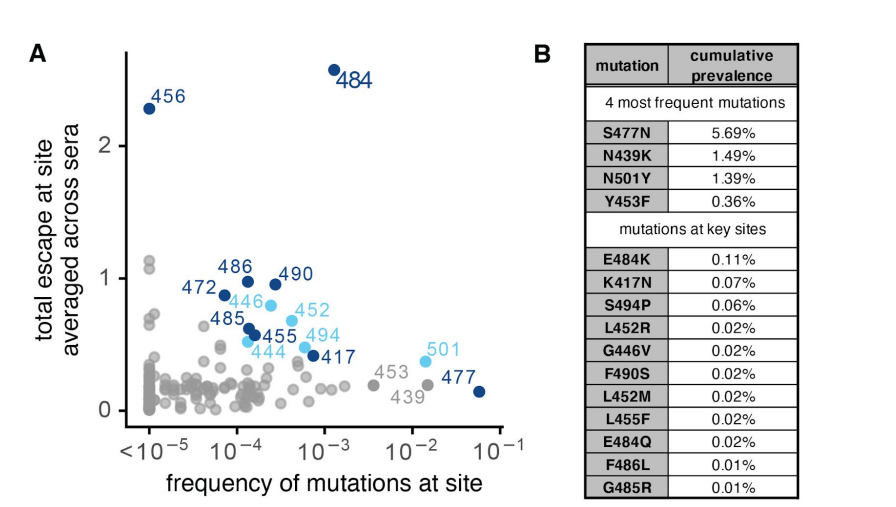
图5. 实验筛选出的RBD免疫逃逸位点在真实世界中的突变频率
总结
这项研究的关键部分使用了ACROBiosystems提供的预偶联RBD蛋白磁珠(Cat.No.MBS-K002)捕获血清中的抗体,实现了快速、彻底的RBD抗体分离。
该款产品是将生物素化的RBD蛋白偶联到具有超顺磁性的链霉亲和素 (SA) 磁珠上,利用链霉亲和素-生物素(SA-Biotin)系统的高结合亲和力(K=10^-15),实现高效率的抗体捕获和筛选,帮助研究人员简便实验过程、缩短实验周期、降低实验成本,奠定了实验成功的基础。
除了该款产品,ACROBiosystems基于独特的生物素化标记蛋白,已推出一系列预偶联新冠抗原的磁珠产品。我们的磁珠由具有超顺磁性的微米级氧化铁颗粒组成,通过表面偶联不同的蛋白,可以特异性结合不同生物配体并实现快速、高效的磁性分离。
磁珠的使用步骤十分简便,通常由孵育、磁分离、洗脱三步组成,只要利用外加磁场就可以进行独立于生物反应的操作,适用于多种实验应用,例如抗体捕获/筛选、病毒富集、细胞分选等。
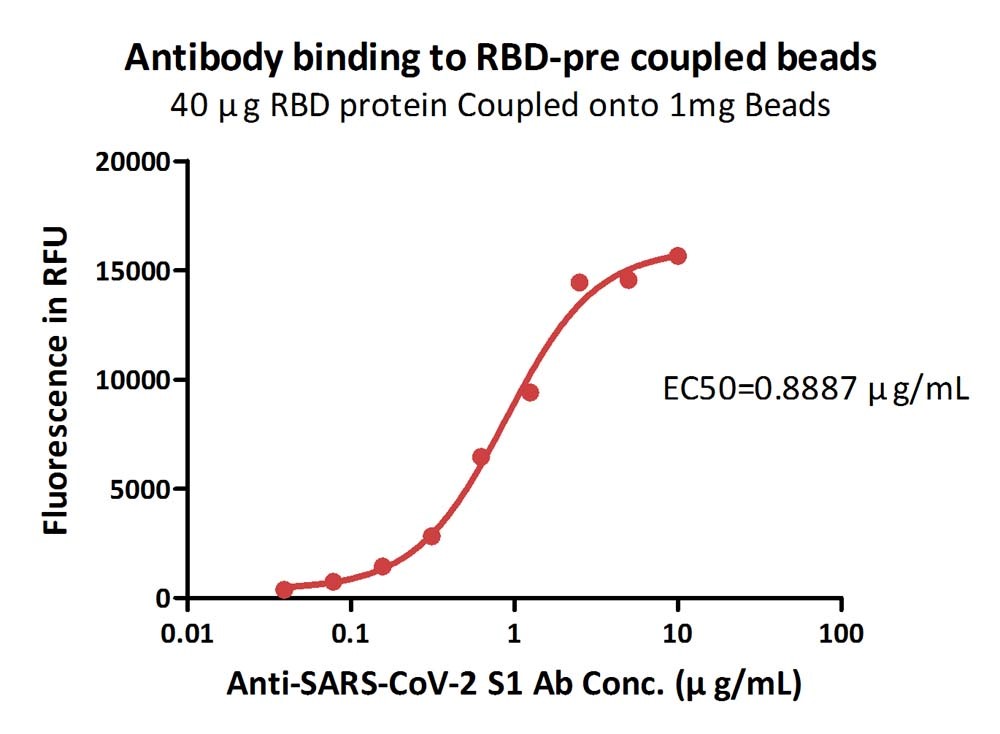
Immobilized 40 μg SARS-CoV-2 S protein RBD/1 mg beads can bind the Anti-SARS-CoV-2 Spike S1 Antibody with an EC50 of 0.8887 μg/mL (QC tested).
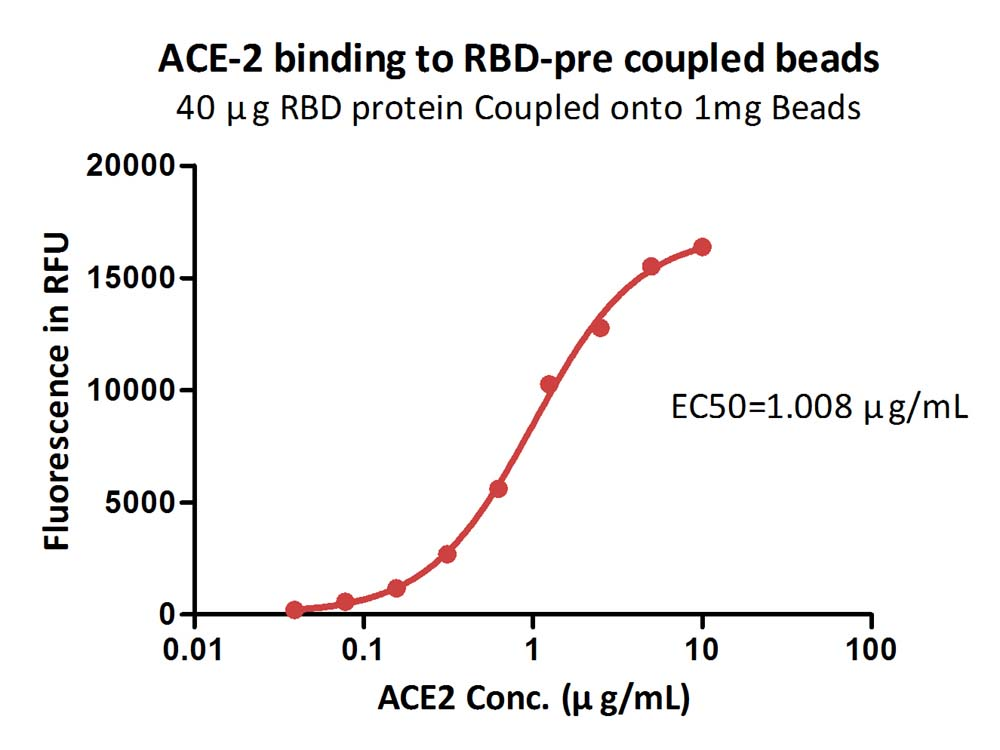
Immobilized 40 μg SARS-CoV-2 S protein RBD/1 mg beads can bind the Human ACE2, Fc Tag (AC2-H5257) with an EC50 of 1.008 μg/mL (QC tested).
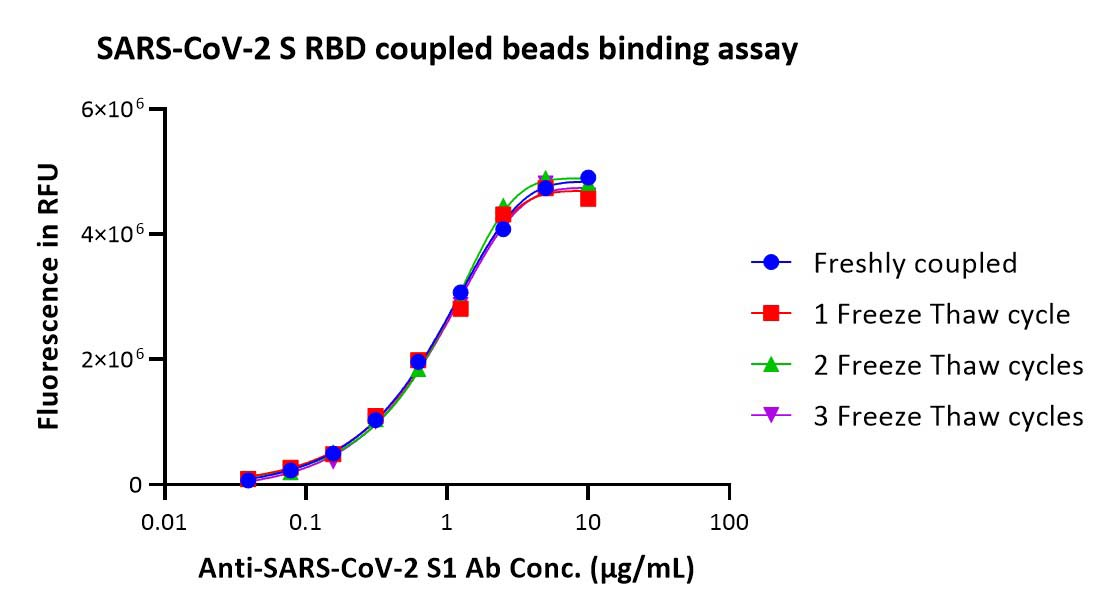
The binding curves between SARS-CoV-2 S RBD pre-coupling magnetic beads (Cat. No. MBS-K002) and anti-SARS-CoV-2 S1 antibody after different freeze-thaw cycles.
点击申请protocol
新冠类磁珠产品列表
>>>>突变株相关预偶联磁珠产品
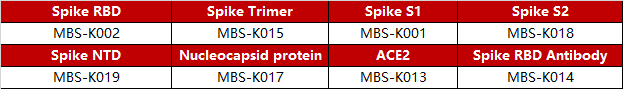
>>>>其他新冠相关预偶联磁珠产品
>>>>点击查看更多其他预偶联磁珠产品
参考文献:
Greaney A. J., Loes A. N., Crawford K. H.D., et al. 2021. Comprehensive mapping of mutations to the SARS-CoV-2 receptor-binding domain that affect recognition by polyclonal human serum antibodies. Cell Host & Microbe. doi: 10.1016/j.chom.2021.02.003

您可通过以下方式联系到ACROBiosystems:
邮件:inquiry@acrobiosystems.com
电话:15117918562
(备注:姓名+公司)